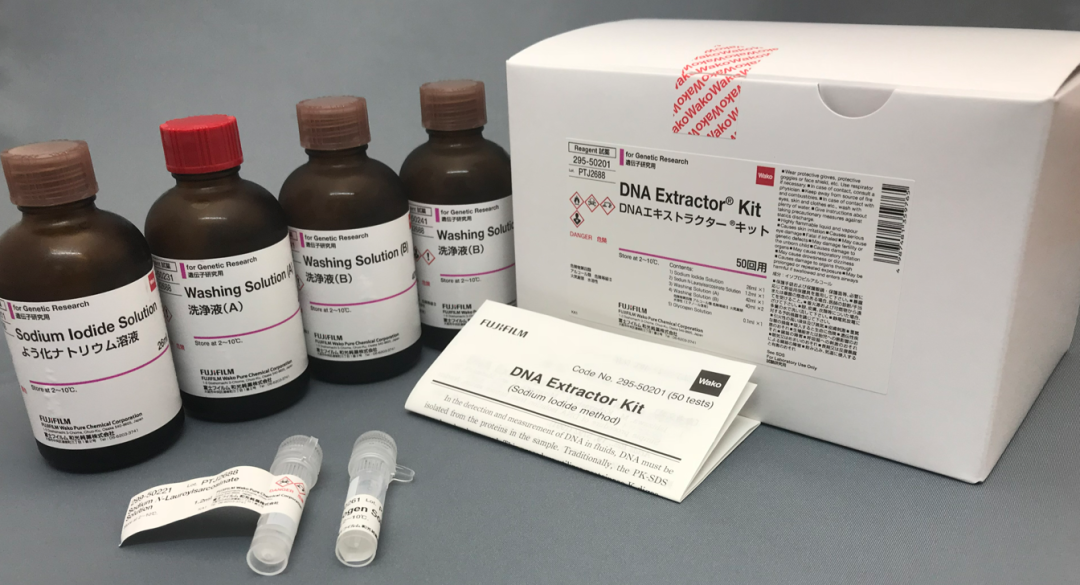
【Wako】生物制药残留DNA提取试剂盒:中国药典登载的碘化钠法
残留DNA提取试剂盒遵照中国药典记载的碘化钠法,适用于疫苗和治疗用生物制品所含宿主细胞残余DNA的提取。
残留DNA提取试剂盒可以提取样品中含有的极微量的DNA,回收率较高。DNA的提取操作时间为60-90 min。提取的DNA可以通过qPCR进行定量。
特点
● 高回收率回收微量DNA(100-1,000 fg)
● 无需更换试管(全程仅使用1根试管)
● 整个提取过程仅需60-90 min
● 提供高浓度蛋白样品的前处理实验方案
● 回收后的DNA可通过qPCR、Threshold Assay(Molecular Devices)进行定量
● 采用碘化钠法
原理
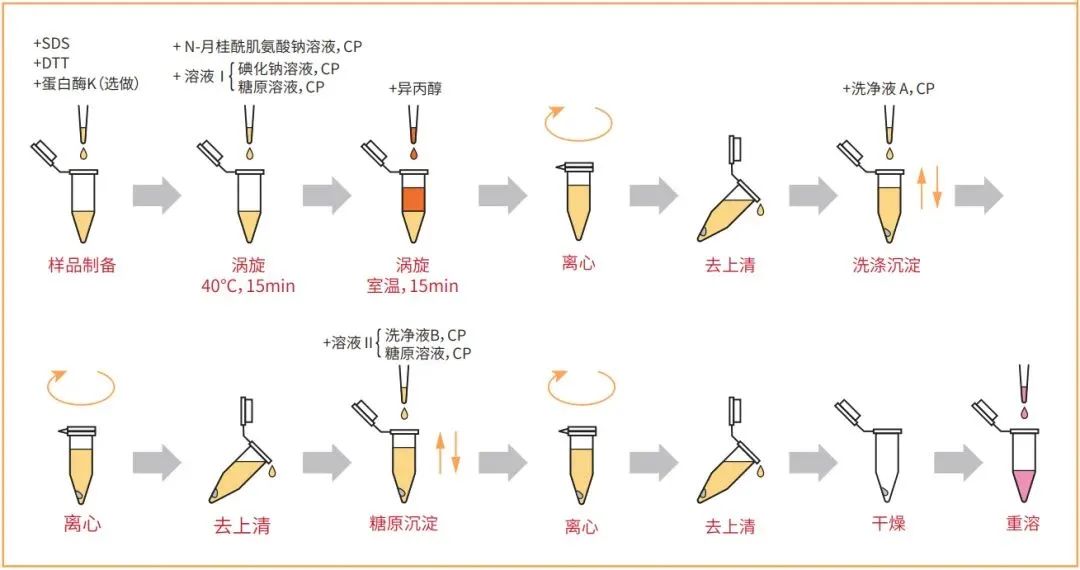
1. 使样品中的蛋白质和脂质溶于碘化钠和月桂酰肌氨酸钠;
2. 异丙醇与糖原选择性地共沉淀DNA。
标准步骤
应用实例
DNA spiking test(加标回收实验)
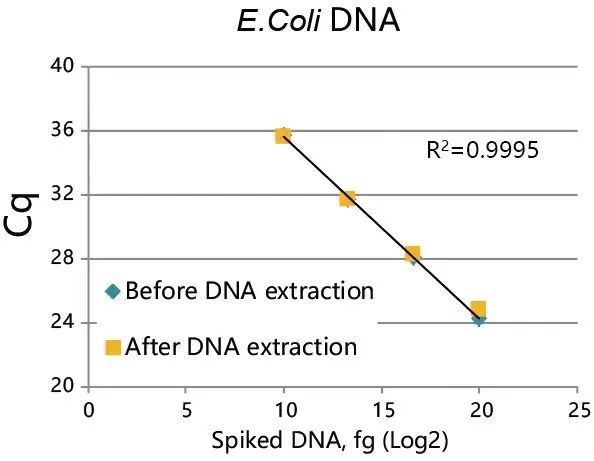
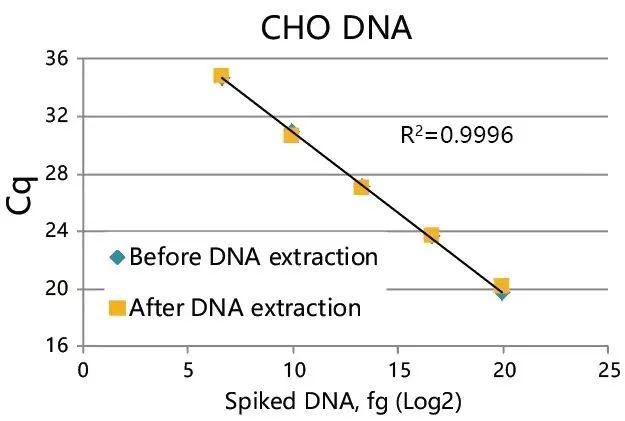
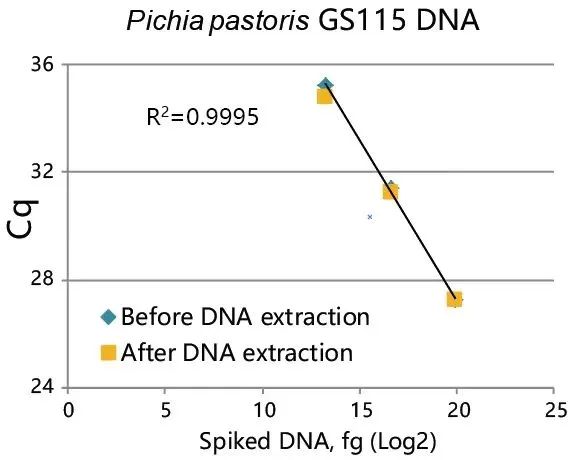
DNA Extractor™ Kit可以高产量提取残留DNA,甚至少量残留DNA。
抗体药物适用性研究
从高蛋白溶液中提取DNA
使用不同浓度的IgG溶液检测CHO来源DNA的加标回收率。
方法
1)向不同浓度的IgG溶液(10-100 mg/mL)中添加2 pg/mL CHO来源DNA。
2)按照本产品说明书记载的实验方案提取DNA。
● 提取实验方案:Protocol#2
● 样品前处理:蛋白浓度超过2 mg/mL时实施的前处理方案(Proteinase K处理)
3)通过qPCR法计算提取的CHO来源DNA的回收率。
结果
不同蛋白浓度溶液的Cq值
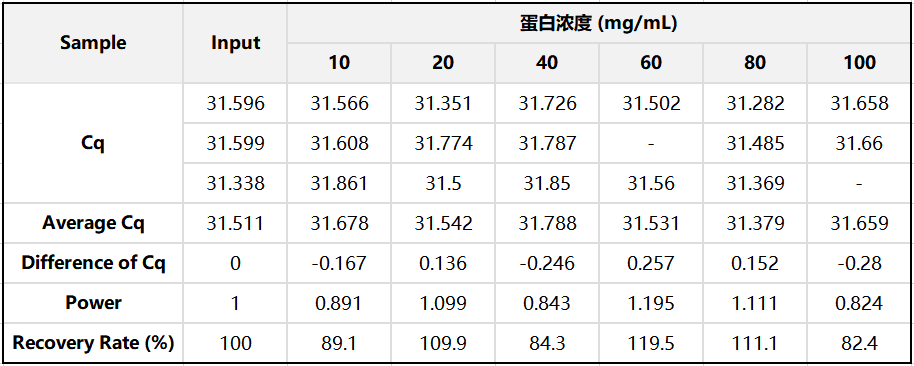
不同蛋白浓度溶液的CHO来源DNA回收率
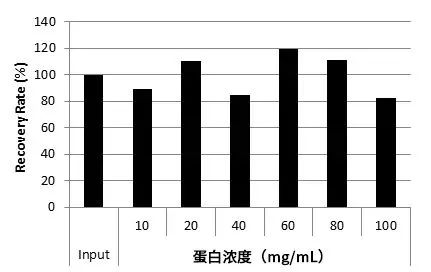
结果显示,即使蛋白浓度高达100 mg/mL,也能高回收率提取CHO来源DNA。
从抗体药物模拟溶液中提取 DNA
检测抗体药物常用的Buffer及添加剂制备的IgG溶液中的 CHO来源DNA的加标回收率。
方法
1)向抗体药物中常用的Buffer组成(表1.①-⑥)及添加剂溶液中添加20 mg/mL的IgG蛋白,制备不同的抗体药物模拟溶液。向不同溶液中添加 20 pg/mL CHO来源DNA。
2)根据本产品说明书记载的实验方案提取DNA。
● 提取实验方案:Protocol#2
● 样品前处理:蛋白浓度超过2 mg/mL时实施的前处理方案(Proteinase K处理)
3)通过qPCR法计算提取的CHO来源DNA的回收率。
表1 Buffer组成

表2 添加剂溶液
Buffer: 10 mM PB pH 6.0, 0.15 M NaCl, 2 mM EDTA

结果
不同Buffer的Cq值

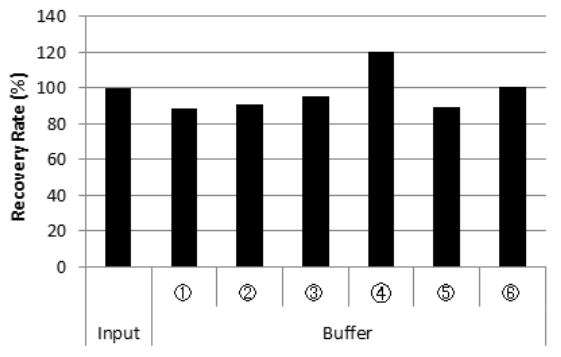
不同Buffer的CHO来源DNA回收率
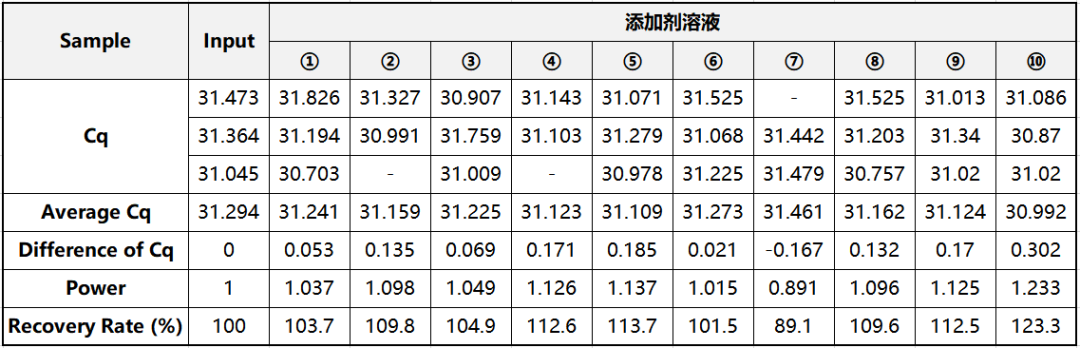
不同添加剂溶液的Cq值
不同添加物溶液的CHO来源DNA回收率
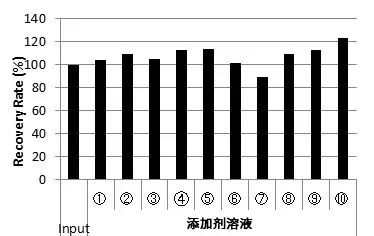
结果显示,即使含有不同Buffer组成和添加剂的IgG溶液也能高回收率提取CHO来源DNA。
产品列表

相关产品

※ 仅供实验研究用,不可用于临床诊断。
点在看,传递你的品味