细胞毒性CD4+T细胞通过靶向巨细胞病毒抗原消除衰老细胞
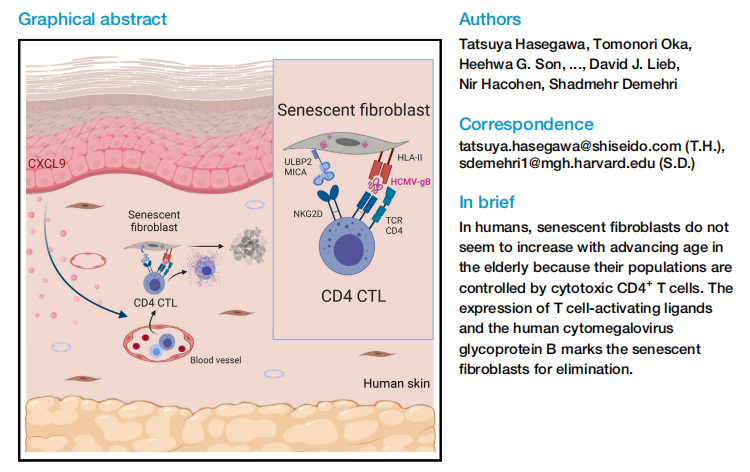
衰老细胞是细胞在应激状态下形成的增殖不可逆停滞但抵抗凋亡的细胞,随年龄增长在体内积累。这类细胞并非惰性,可通过分泌炎症因子、组织重塑因子等组成的衰老相关分泌表型(SASP),引发组织慢性炎症,进而参与癌症、退行性疾病等衰老相关病症的发生发展,因此清除异常积累的衰老细胞对维持组织稳态、延长健康寿命具有重要意义。
已有研究证实,通过基因或药物手段清除小鼠体内的衰老细胞,可恢复组织稳态并延长健康寿命。但目前这类方法存在明显缺陷:一方面会产生显著副作用,另一方面缺乏长期耐久性,难以应用于人类临床场景,因此亟需探索更安全、有效的清除机制。
当前衰老细胞相关研究多依赖小鼠模型,但小鼠与人类的衰老细胞在形成机制(如端粒缩短、氧化应激的作用)、表型特征上存在本质区别。更关键的是,小鼠缺乏人类长期暴露的病原体环境,免疫监视机制与人类进化差异显著,无法完整复刻人类对衰老细胞的免疫应答过程,导致基于小鼠模型的研究结果难以直接推广至人类。
在小鼠模型中,衰老细胞可通过表达免疫调节分子、所处微环境中的免疫抑制因子等逃避免疫清除,但人类衰老器官中,免疫系统如何调控衰老细胞积累的具体机制尚不明确。尤其是人类皮肤作为易观察、易获取的衰老相关器官,其内部衰老细胞(如成纤维细胞)的清除机制缺乏系统研究,存在明显的科学空白。
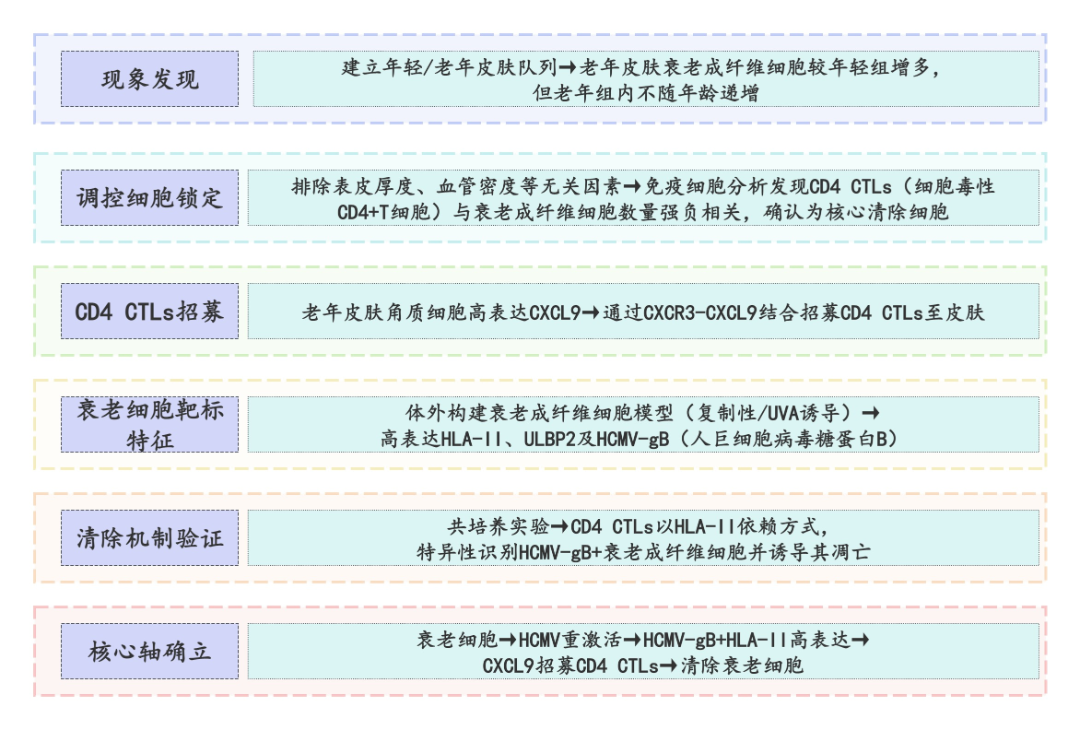
发现老年皮肤中衰老成纤维细胞较年轻皮肤增多,但老年群体内该细胞数量不随年龄递增,提示存在调控机制;排除表皮厚度、血管密度等无关因素后,锁定CD4 CTLs(细胞毒性CD4+T细胞)为核心清除细胞,其数量与衰老成纤维细胞积累呈强负相关;进一步发现老年皮肤角质细胞高表达CXCL9,可通过与CD4 CTLs表面CXCR3结合招募该细胞至皮肤;
体外构建衰老成纤维细胞模型证实其高表达HLA-II、ULBP2及HCMV-gB抗原,体内实验验证这类标记阳性细胞在老年皮肤中显著增多;通过共培养、抗体阻断等实验,证实CD4 CTLs以HLA-II依赖方式清除衰老成纤维细胞,且HCMV-gB是其特异性识别的关键抗原;
最终提出“衰老细胞→HCMV重激活→HCMV-gB+HLA-II高表达→CXCL9招募CD4 CTLs→特异性清除”的病毒-免疫调控轴,揭示HCMV在衰老细胞免疫监视中的共生样功能。
1. 老年人皮肤中的衰老细胞数量增多
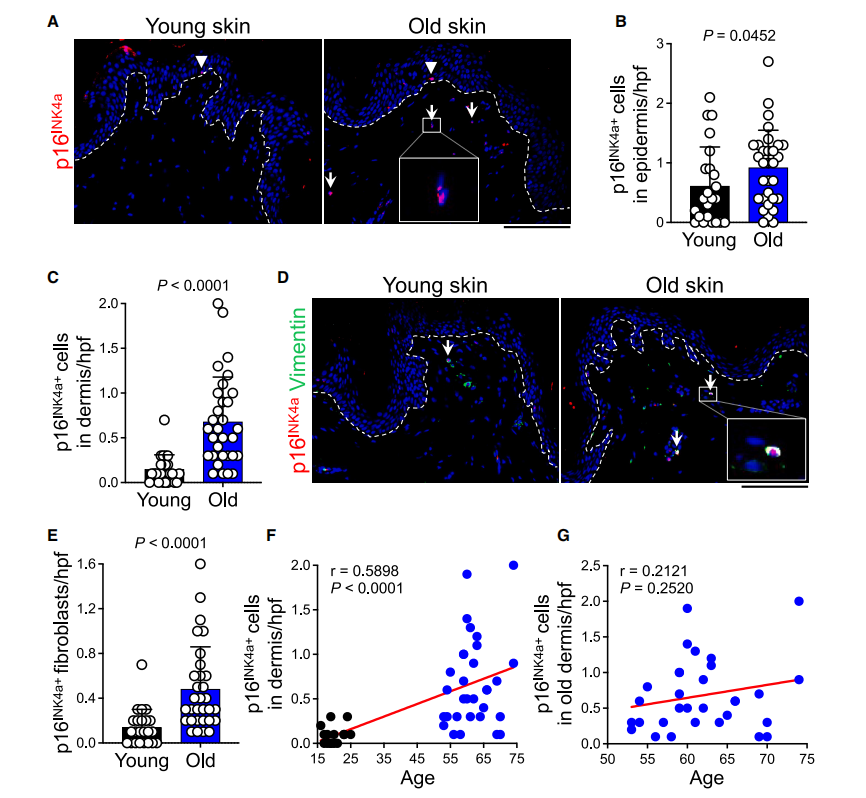
研究筛选 800 余例不同年龄、解剖部位的人类皮肤样本,排除紫外线辐射、性别差异等干扰因素后,建立年轻组(n=23,平均年龄 23.1 岁)和老年组(n=31,平均年龄 62.1 岁)女性防晒躯干皮肤队列。
通过免疫荧光染色检测 p16INK4a、p21、SenTraGor 等衰老标志物,并结合 vimentin(成纤维细胞标志物)、PDGFRα 鉴定细胞类型,发现老年皮肤的表皮和真皮中,衰老细胞数量均显著高于年轻皮肤,且真皮中衰老细胞增多的幅度更明显。
进一步分析表明,真皮中 80% 以上的衰老细胞为成纤维细胞,但老年组内部,衰老成纤维细胞的数量与年龄无显著相关性(r=0.2121,p=0.2520),提示存在调控其积累的生物学机制。
2. 细胞毒性 CD4+T 细胞(CD4 CTLs)是衰老人类皮肤中主要的细胞毒性淋巴细胞
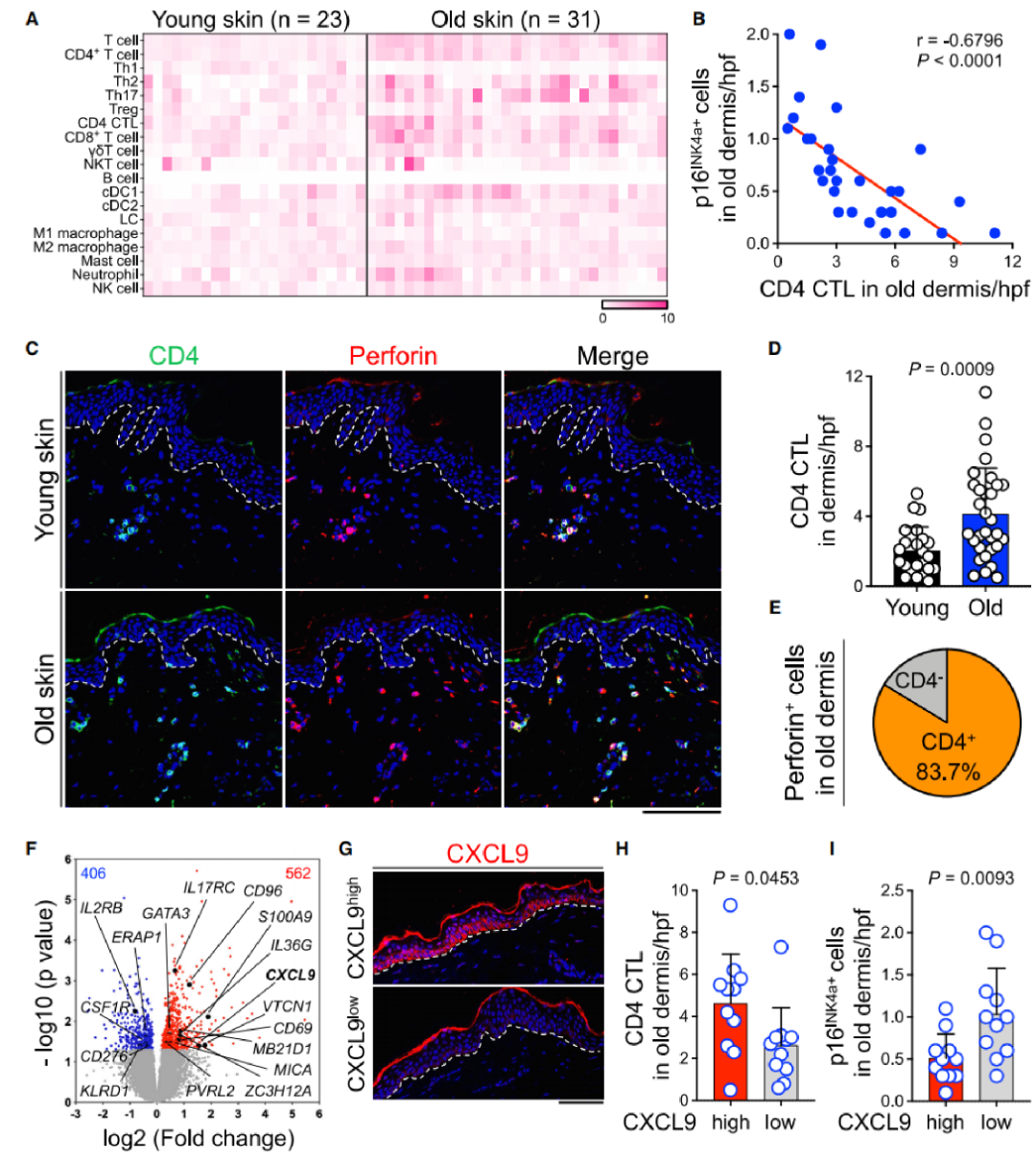
通过多重免疫染色、单细胞 RNA 测序(scRNA-seq)对老年皮肤免疫细胞进行分析,发现 CD4 CTLs(以穿孔素表达为标记)在老年皮肤真皮层中显著富集,占真皮层穿孔素阳性细胞的 83.7%,是该部位主要的细胞毒性淋巴细胞。
进一步研究显示,CD4 CTLs 高表达 CD69(驻留记忆标志物)及 RUNX3、RAB27A 等细胞毒性相关基因,且其数量与老年皮肤中衰老成纤维细胞的积累呈强负相关(r=-0.6796,p<0.0001),明确其为调控衰老细胞积累的关键效应细胞。
3. 细胞毒性 CD4+T 细胞(CD4 CTLs)可直接靶向衰老成纤维细胞
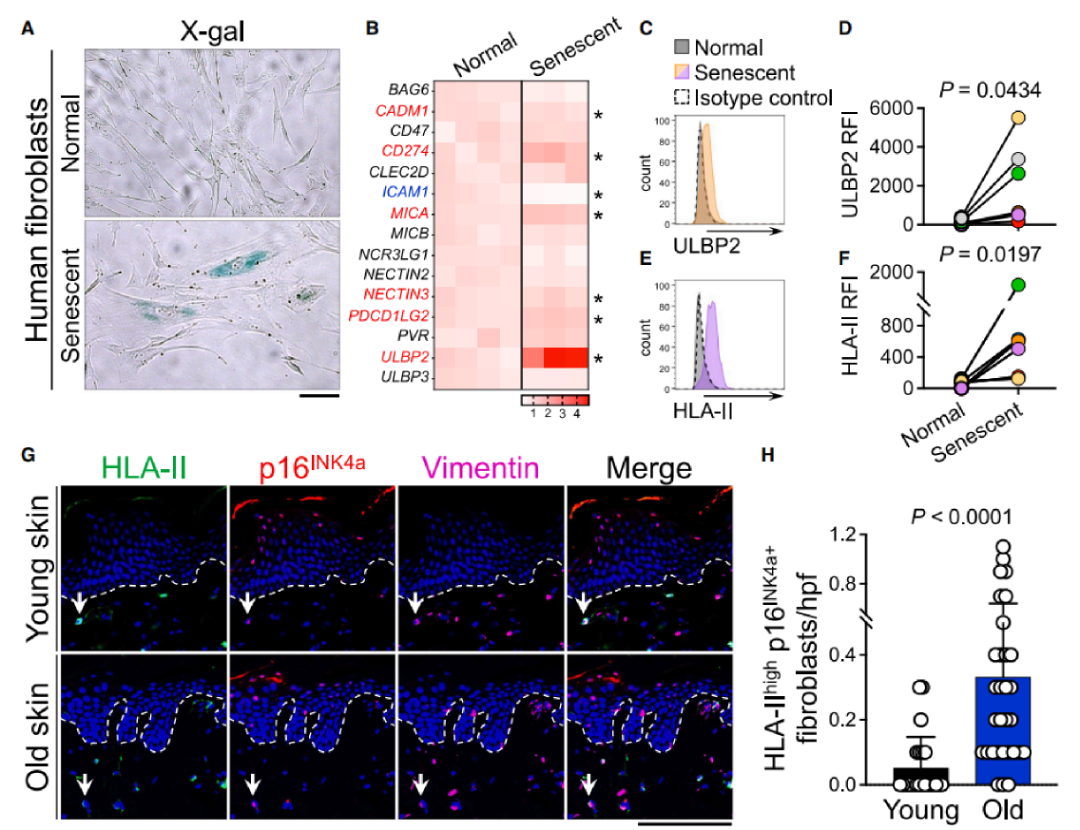
通过反复传代(复制性衰老)、UVA 照射(5/10 J)体外构建衰老成纤维细胞模型,经衰老相关 β- 半乳糖苷酶(SA-β-Gal)染色验证衰老表型。RNA-seq 分析与流式细胞术检测发现,衰老成纤维细胞高表达 ULBP2(NKG2D 配体)、人类白细胞抗原 II 类分子(HLA-II)等免疫识别相关配体,而正常成纤维细胞中这些分子表达可忽略。
体内实验进一步证实,老年皮肤中 HLA-II 高表达、ULBP2 阳性的衰老成纤维细胞数量显著高于年轻皮肤,且这类细胞所在的皮肤样本中 CD4 CTLs 数量更多,为 CD4 CTLs 直接识别衰老成纤维细胞提供了分子基础。
4. 细胞毒性 CD4+T 细胞(CD4 CTLs)以人类白细胞抗原 II 类分子(HLA-II)依赖的方式清除衰老成纤维细胞
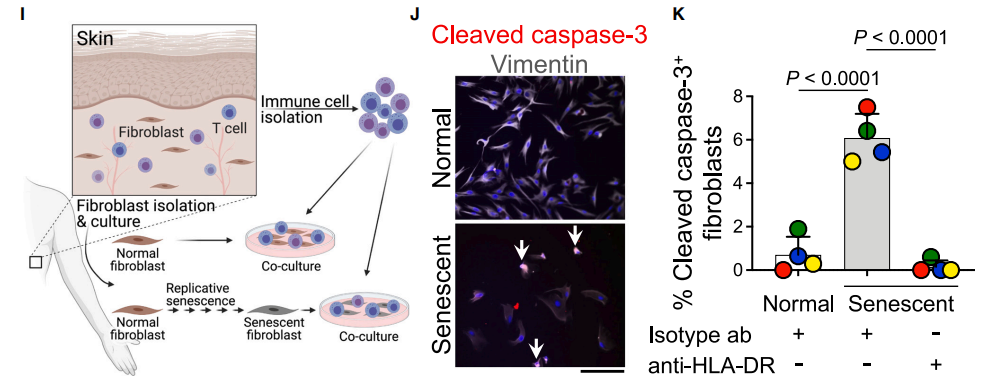
共培养实验证实 CD4 CTLs 可特异性诱导衰老成纤维细胞凋亡,该效应会因 HLA-II 功能阻断或表达下调而受抑;且共培养后 CD4 CTLs 的脱颗粒、激活标志物表达上调,明确其清除作用依赖 HLA-II 分子。
5. 细胞毒性 CD4+T 细胞(CD4 CTLs)通过靶向人巨细胞病毒糖蛋白 B(HCMV-gB)抗原清除衰老成纤维细胞
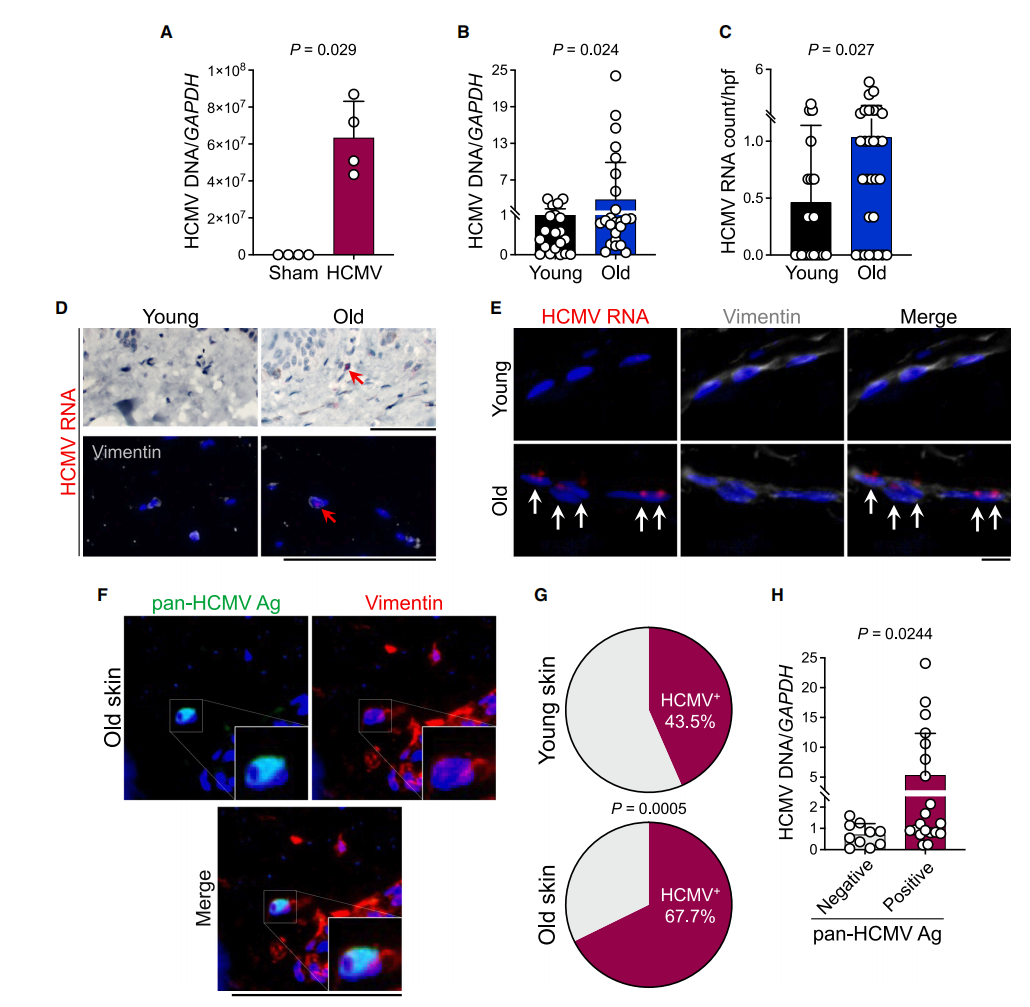
为探究触发 CD4 CTL 杀伤衰老成纤维细胞的 HLA-II 结合抗原,研究锁定人巨细胞病毒糖蛋白 B(HCMV-gB),该抗原是 CD4+T 细胞的主要靶标,95% 健康人血液中均存在其特异性 CD4+T 细胞。
本研究的皮肤供体为美国人,HCMV 在该人群中高度流行,其中研究涉及的老年皮肤供体队列(平均 62.1 岁)血清阳性率超 90%,显著高于年轻人群。实验检测发现,正常人体皮肤中可检测到 HCMV 的 DNA 和 RNA,且老年皮肤中的二者含量显著高于年轻皮肤,老年皮肤的真皮成纤维细胞中 HCMV RNA 的表达尤为明显。
研究还通过临床级泛 HCMV 抗原抗体鸡尾酒检测皮肤样本的 HCMV 感染状态,发现 67.7% 的老年皮肤样本、43.5% 的年轻皮肤样本中存在 HCMV 阳性真皮细胞,这一结果与美国人群的 HCMV 血清阳性率分布相符;同时还发现,泛 HCMV 抗原阳性的皮肤样本,其内部的 HCMV DNA 水平也相对更高。
6. 细胞毒性 CD4+T 细胞(CD4 CTLs)通过靶向人巨细胞病毒糖蛋白 B(HCMV-gB)抗原清除衰老成纤维细胞
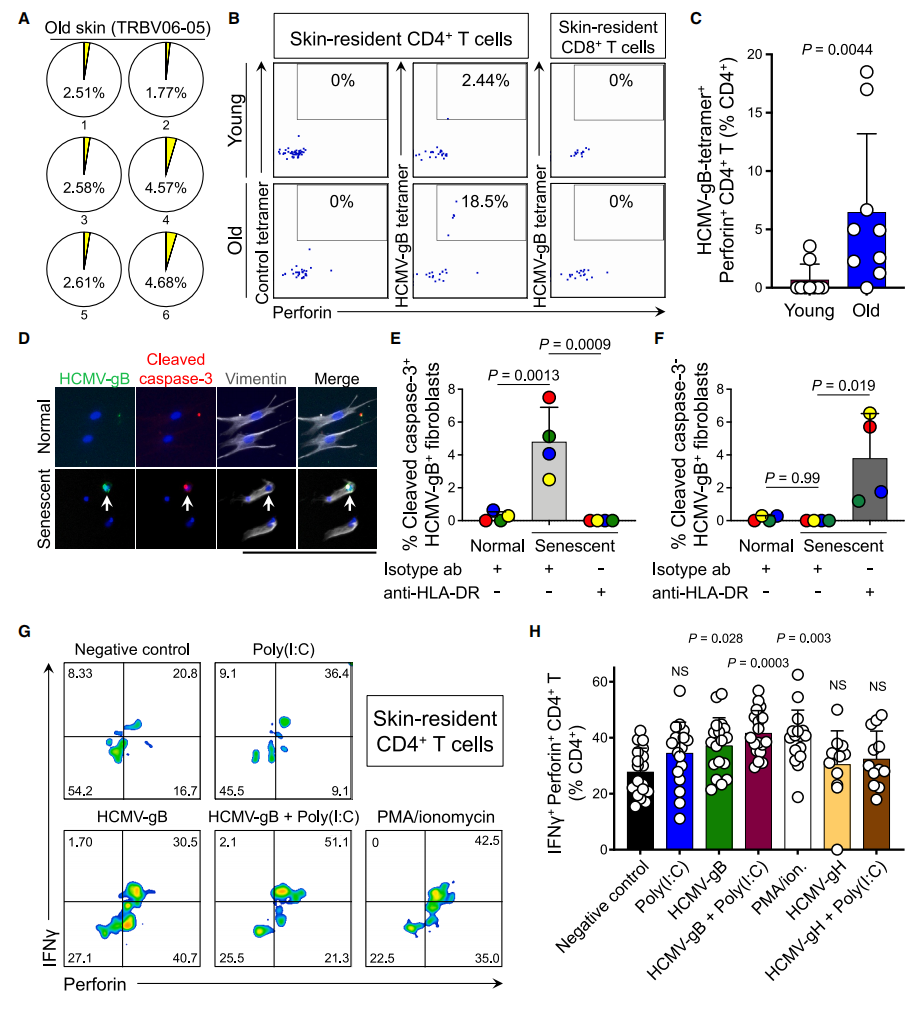
(1)表达TCRβ链TRBV6-5的CD4 CTLs可识别HLA-DRB107:01呈递的HCMV-gB表位,对该基因型的老年皮肤进行TCR测序,检测到了这类T细胞克隆;
(2)利用含HCMV-gB衍生肽的HLA-肽四聚体染色,进一步证实老年皮肤中存在HCMV-gB特异性CD4 CTLs;
(3)泛HCMV抗原阳性皮肤样本的自体共培养实验显示,大部分凋亡的衰老成纤维细胞均表达HCMV-gB,且HLA-DR阻断后,HCMV-gB+衰老成纤维细胞可免于被杀伤;
(4)体外实验发现,重组HCMV-gB能诱导皮肤穿孔素+CD4 CTLs表达IFNγ,联合可增强皮肤抗原提呈细胞激活的poly(I:C)时,该诱导效果更显著,而HCMV-gH联合poly(I:C)则无法诱导CD4 CTLs表达IFNγ。
1. 核心机制:CD4 CTLs经CXCL9募集至老年皮肤,以HLA-II依赖方式,识别衰老成纤维细胞中再激活的HCMV-gB将其清除,这也解释了老年皮肤衰老成纤维细胞未随年龄线性增加的原因,且HCMV在免疫健全宿主中对衰老细胞免疫监视具有共生作用。
2. 细胞水平意义:CD4 CTLs是老年皮肤主要的细胞毒性淋巴细胞,超级百岁老人体内该细胞大量富集,推测其除抗病毒外,还通过清除衰老细胞助力超长寿命。
3. 病毒特性:HCMV在免疫健全者中终身潜伏,其特异性CD4 CTLs高细胞毒性、低炎症;衰老成纤维细胞中HCMV呈流产复制,仅高表达gB,且细胞衰老可克服HCMV对HLA-II的表达抑制,固有与适应性免疫或协同参与衰老细胞清除。
4. 生物学功能:细胞衰老是天然抗病毒防御机制,既抑制HCMV裂解扩散,又为免疫清除提供靶标,维持病毒定植器官的稳态。
5. 应用启示:证实人类免疫系统与HCMV的共生进化关系,提出研发HCMV抗原疫苗增强相关T细胞免疫,实现衰老细胞特异性清除,为干预衰老相关疾病提供新策略。
6. 研究局限:所用皮肤样本无法确定供体HCMV血清状态;缺乏体内实验验证该机制对衰老相关疾病的抑制作用;尚未开展人类前瞻性临床试验证实其治疗价值。