氧脂素的生物合成促进细胞衰老并实现对衰老细胞清除的检测
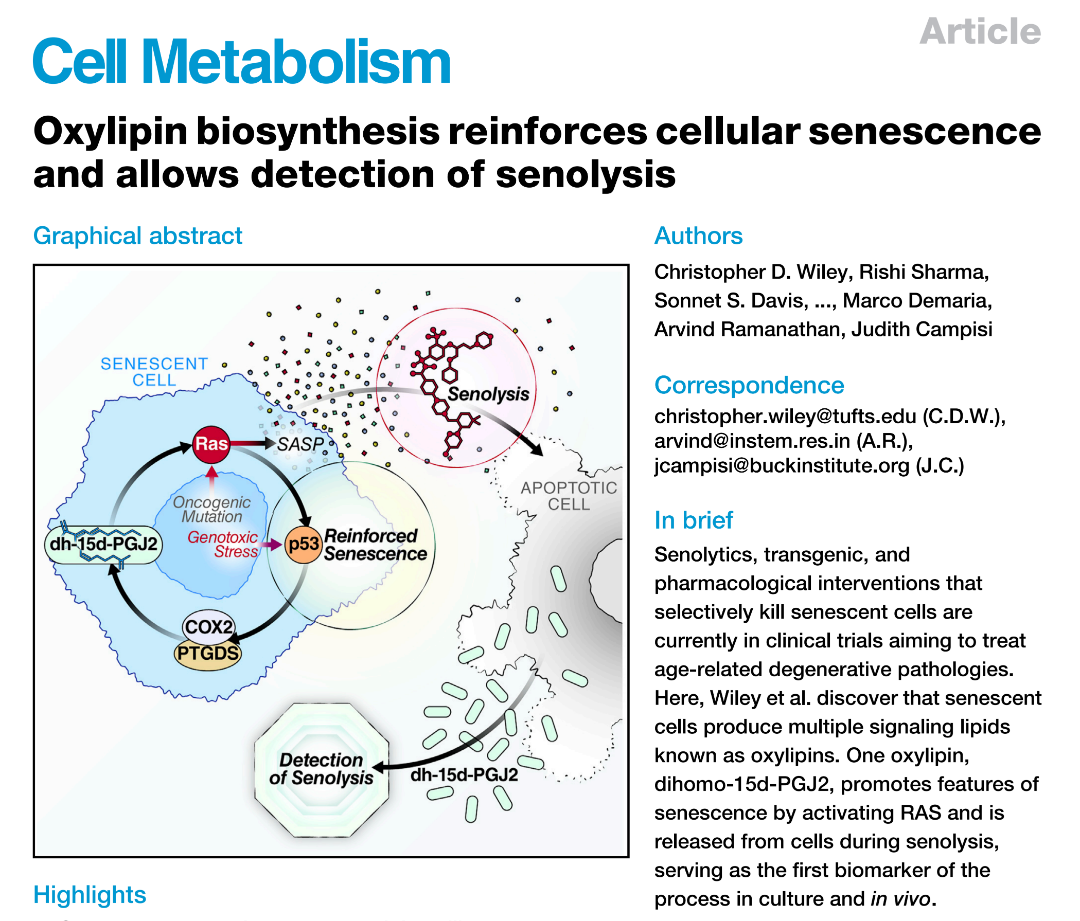
靶向清除衰老细胞的衰老细胞清除剂、转基因及药理学干预手段,目前正处于治疗年龄相关退行性疾病的临床试验阶段。本研究中,威利团队发现衰老细胞可产生多种名为氧脂素的信号脂质,其中二高-15d-前列腺素J2这一氧脂素能通过激活RAS信号通路促进细胞衰老表型的形成,且该物质会在衰老细胞清除过程中从细胞内释放,成为首个能在体外细胞培养及动物体内检测这一过程的生物标志物。
《CellMetabolism》2021年4月 IF30.9
胞衰老是机体应对应激或损伤时启动的一种多维度应答状态,其核心特征表现为不可逆的增殖停滞及衰老相关分泌表型。衰老细胞随年龄增长在组织中不断累积,通过其分泌活动驱动多种年龄相关疾病的发生发展。靶向清除衰老细胞的Senolytics疗法已在临床前研究中显示出延长健康寿命的潜力,然而,由于缺乏特异便捷的疗效检测标志物,其临床转化与应用仍面临瓶颈。
长期以来,SASP的功能研究主要聚焦于炎症细胞因子、蛋白酶等分泌型蛋白质,而其脂质成分的研究几乎处于空白。尽管已有研究发现衰老细胞可产生少量特定脂质,但对衰老相关脂质图谱、功能及调控网络的系统认知仍十分匮乏。脂氧素作为多不饱和脂肪酸来源的生物活性脂质,虽已知其参与调控炎症与纤维化过程,且合成酶活性曾被报道与衰老存在微弱关联,但其在细胞衰老中的具体作用、合成机制及调控通路至今未被揭示。
在分子层面,RAS与p53是调控细胞衰老的核心信号通路。癌基因RAS突变或p53激活均可诱导衰老发生,然而,脂质分子是否参与RAS/p53通路的衰老维持调控,以及是否存在脂质与这一通路的反馈调控网络,仍是亟待解决的关键科学问题。解析这一网络不仅有助于深入理解衰老的脂质代谢调控机制,也可能为Senolytics疗效评估提供全新的液体活检标志物。
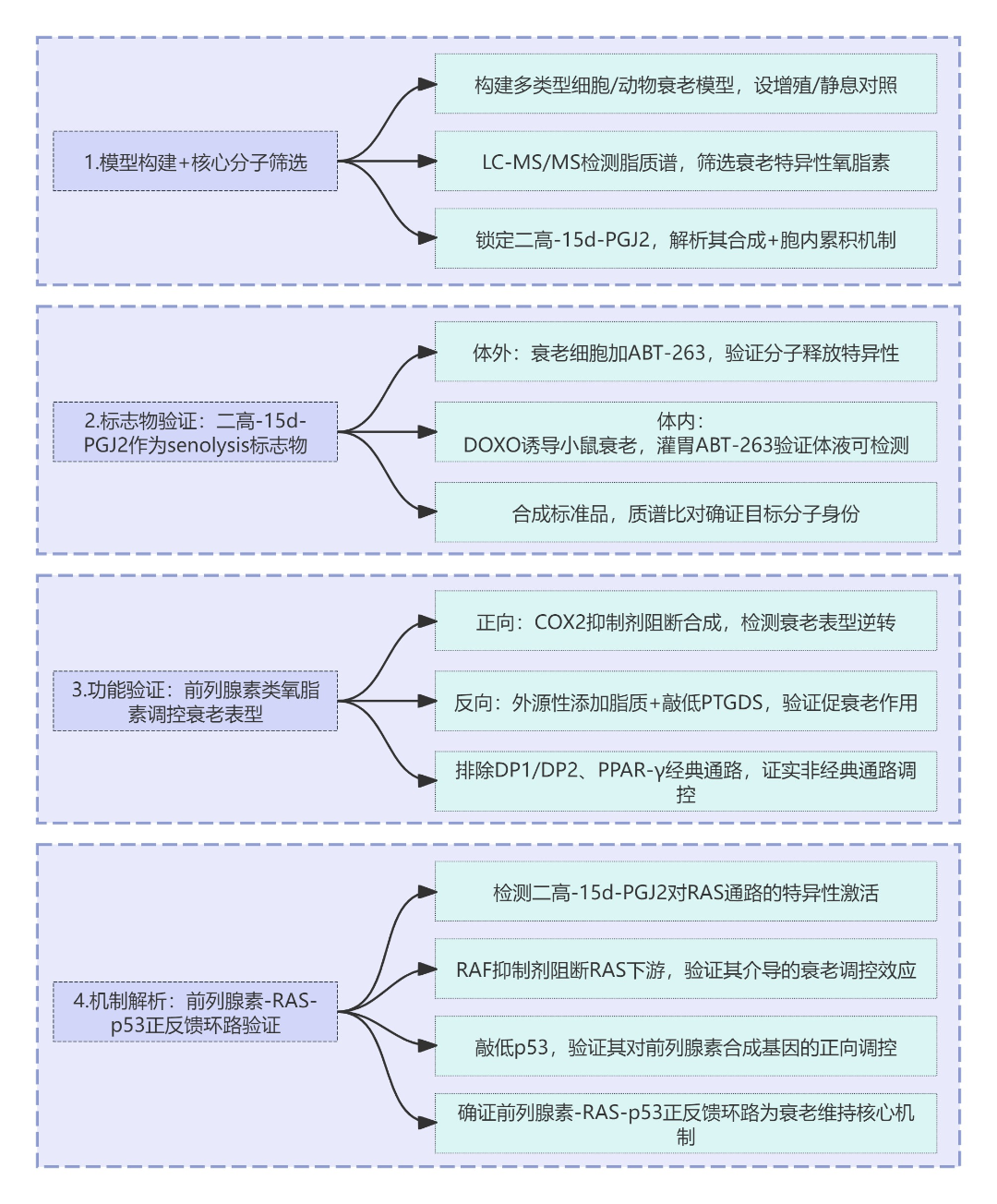
1.筛分子:构建多类型细胞/动物衰老模型,通过脂质谱分析筛选出衰老细胞特异性合成累积的氧脂素,锁定二高-15d-PGJ2为核心分子,解析其合成及胞内累积机制。
2.验标志物:结合体外细胞、体内动物实验,验证二高-15d-PGJ2在衰老细胞清除中特异性释放的特征,确证其作为senolysis标志物的可行性。
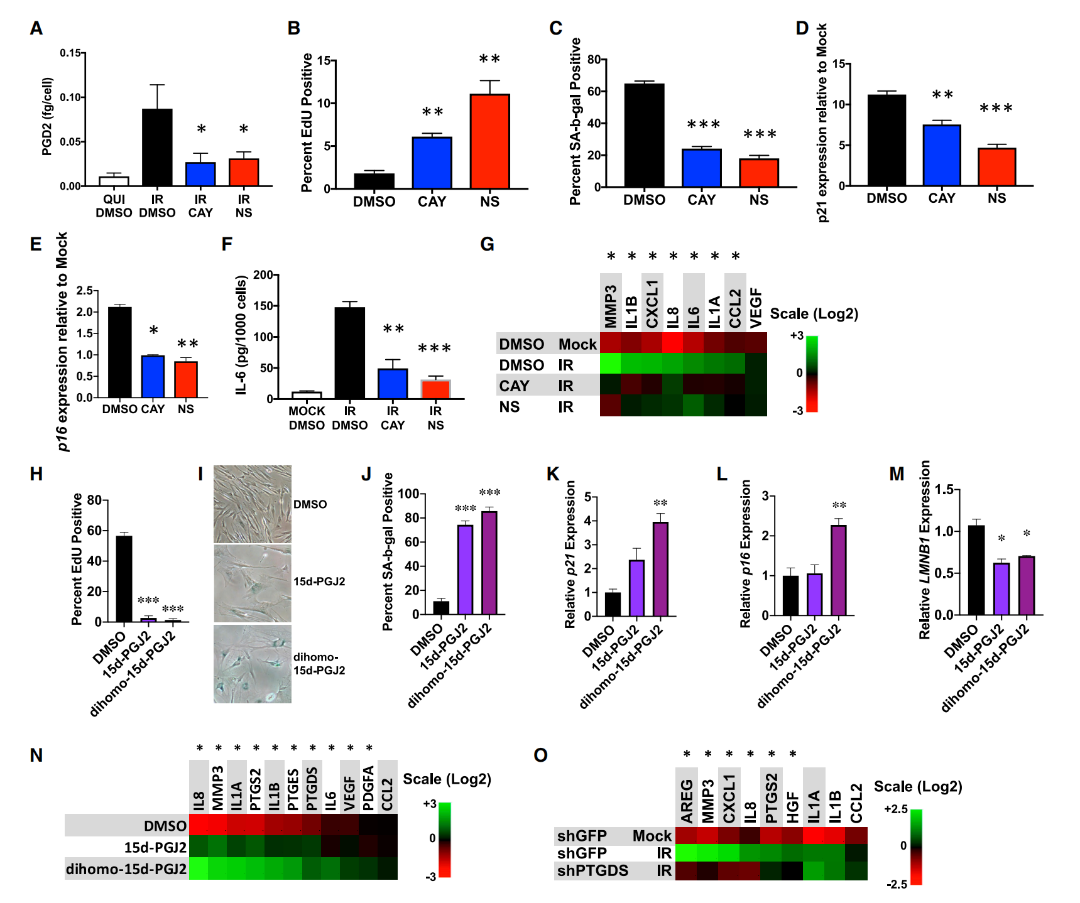
3.证功能:通过抑制剂阻断、外源性添加、基因敲低等正反实验,验证前列腺素类氧脂素对细胞衰老增殖停滞和炎症性SASP的正向调控作用,排除经典信号通路。
4.析机制:聚焦RAS/p53信号轴,经通路激活检测、抑制剂阻断、基因敲低等实验,证实前列腺素-RAS-p53正反馈环路是维持细胞衰老的核心分子机制。
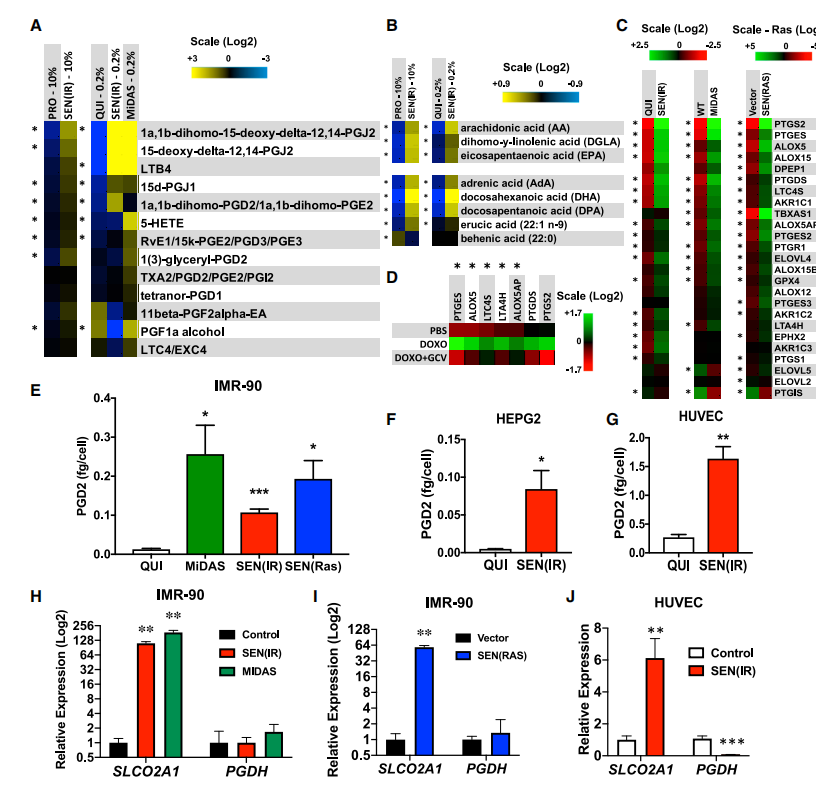
本部分通过细胞与动物实验结合脂质谱分析、分子检测,明确了衰老细胞的氧脂素合成特征及机制:
以IMR-90成纤维细胞构建衰老模型,LC-MS/MS检测发现衰老细胞特异性富集多种氧脂素,二高-15d-PGJ2上调最显著,且其相关前体脂肪酸(AA、AdA等20/22碳PUFA)选择性升高;
衰老细胞中氧脂素合成相关基因(COX2、PTGDS、ALOX5等)普遍上调,该结果在多种细胞系及衰老小鼠肝脏中得到验证,且清除衰老细胞可逆转该基因表达变化;
衰老细胞存在PGD2分泌增加的现象,同时前列腺素转运体SLCO2A1大幅上调、降解酶PGDH表达失衡,最终导致氧脂素在衰老细胞内特异性累积,且该合成特征也存在于老年小鼠的组织中。
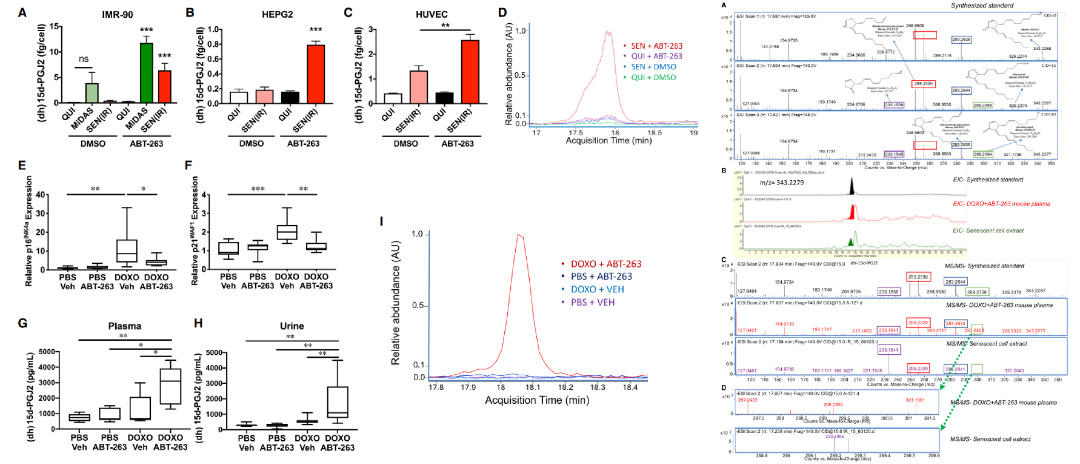
二高-15d-PGJ2是体内外衰老细胞清除的生物标志物
本部分通过体内外实验结合多技术验证,明确二高-15d-PGJ2是衰老细胞清除的首个特异性生物标志物,核心结论如下:
针对二高-15d-PGJ2胞内累积、无基础分泌的特征提出假说,在IMR-90、HEPG2、HUVEC三种衰老细胞模型中,经ABT-263处理后培养基中该分子释放量均显著升高,静息细胞无此变化。
质谱检测证实释放的脂质为二高-15d-PGJ2,且非衰老细胞经普通凋亡诱导剂处理后不释放该分子,明确其与senolysis的特异性关联,与普通细胞凋亡无关。
体内构建DOXO诱导的小鼠衰老模型,灌胃ABT-263后,小鼠衰老标志物p16/p21表达下降,血浆、尿液中二高-15d-PGJ2水平显著升高,且仅senolysis组能检测到该分子的特征质谱峰。
利用人工合成的二高-15d-PGJ2标准品完成质谱比对,目标分子的保留时间、碎片峰与标准品完全一致,精准确证其身份,证实该分子为首个可在体内外检测衰老细胞清除的生物标志物。
本部分通过体内外实验结合多技术验证,明确二高-15d-PGJ2是衰老细胞清除的首个特异性生物标志物,核心结论如下:
针对二高-15d-PGJ2胞内累积、无基础分泌的特征提出假说,在IMR-90、HEPG2、HUVEC三种衰老细胞模型中,经ABT-263处理后培养基中该分子释放量均显著升高,静息细胞无此变化。
质谱检测证实释放的脂质为二高-15d-PGJ2,且非衰老细胞经普通凋亡诱导剂处理后不释放该分子,明确其与senolysis的特异性关联,与普通细胞凋亡无关。
体内构建DOXO诱导的小鼠衰老模型,灌胃ABT-263后,小鼠衰老标志物p16/p21表达下降,血浆、尿液中二高-15d-PGJ2水平显著升高,且仅senolysis组能检测到该分子的特征质谱峰。
利用人工合成的二高-15d-PGJ2标准品完成质谱比对,目标分子的保留时间、碎片峰与标准品完全一致,精准确证其身份,证实该分子为首个可在体内外检测衰老细胞清除的生物标志物。
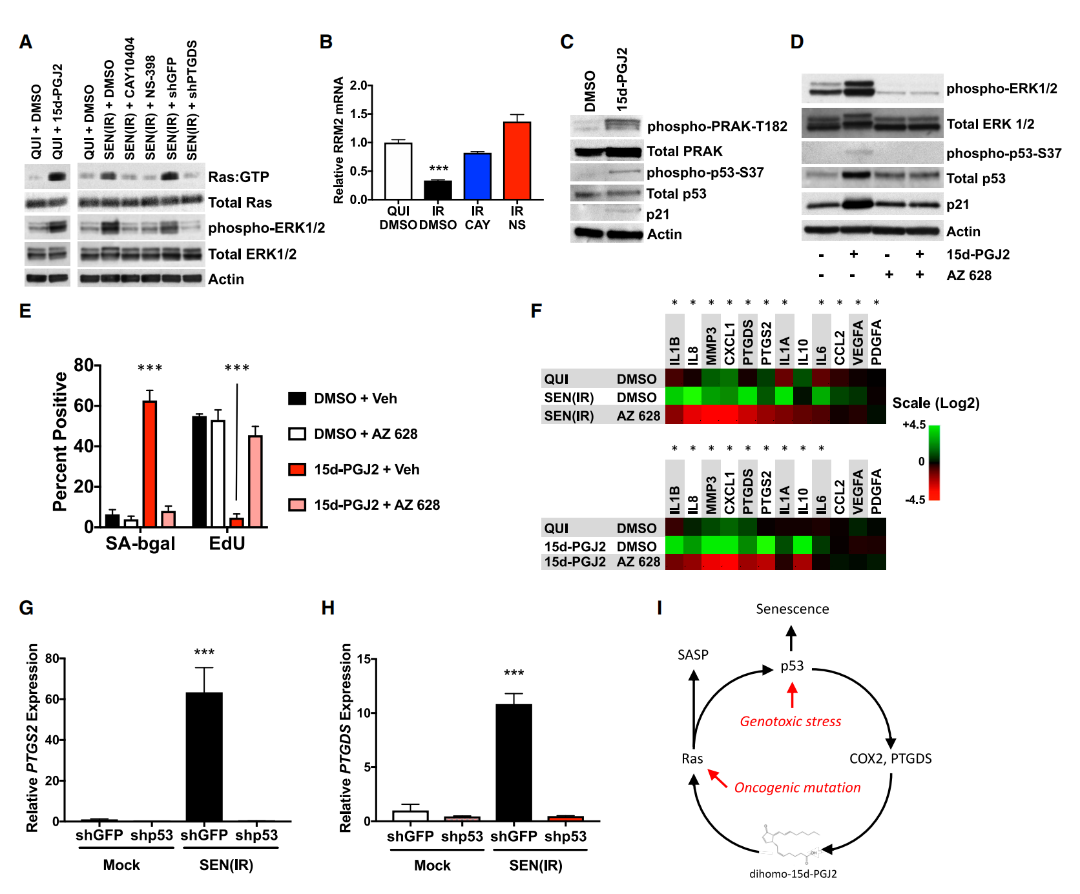
本部分明确了前列腺素强化细胞衰老的核心分子机制为RAS/p53正反馈环路,通过通路激活、抑制剂阻断、基因敲低等实验完成验证,核心结论如下:
二高-15d-PGJ2可特异性激活衰老细胞的RAS通路,使RAS-GTP水平升高、下游ERK1/2磷酸化,COX2抑制剂或PTGDS敲低可抑制该激活效应,证实前列腺素是衰老细胞中RAS通路激活的关键因素。
RAS通路激活通过MAPK/PRAK介导p53Ser37磷酸化并上调p21,进而诱导细胞衰老;采用RAF抑制剂AZ628阻断RAS下游通路,可逆转前列腺素诱导的衰老表型,同时下调前列腺素合成基因,打破其合成正反馈。
p53是前列腺素合成基因(PTGS2/PTGDS)的上游特异性调控因子,敲低p53可完全消除衰老诱导的前列腺素合成基因上调,证实p53对前列腺素合成的正向调控作用;而NF-κB不参与该调控过程。
本研究首次证实衰老细胞中存在前列腺素-RAS-p53正反馈环路:前列腺素激活RAS通路并介导p53激活,激活的p53促进前列腺素合成,进而持续激活RAS通路,形成环路并稳定维持细胞衰老表型,且该环路是衰老维持的关键机制。
填补领域研究空白:首次证实氧脂素是SASP的关键脂质组分,突破SASP研究长期聚焦蛋白质的现状;发现野生型RAS在细胞衰老中的核心调控作用,填补了其在非癌基因诱导衰老中功能的研究空白。
解析核心分子机制:明确衰老细胞中SLCO2A1转运体上调、PGDH降解酶表达失衡,是二高-15d-PGJ2胞内特异性累积的原因;阐释p53对SASP的双重调控作用——既拮抗NF-κB抑制部分SASP,又促进氧脂素合成推动炎症性SASP形成;确证前列腺素-RAS-p53正反馈环路是稳定维持细胞衰老表型的核心机制。
明确生理与临床价值:生理层面,推测衰老细胞合成的氧脂素可能参与分娩等生理过程调控;临床层面,二高-15d-PGJ2作为首个可在体液中检测的senolysis特异性标志物,解决了Senolytics临床疗效监测的技术瓶颈,大幅推动其在年龄相关疾病中的临床转化。
提出动态调控新视角:结合衰老与SASP的动态表型特征,推测氧脂素的合成与调控具有时空依赖性,可能参与衰老表型从急性到慢性应激的转化过程,为后续研究提供新靶点。
客观指出研究局限:一是除二高-15d-PGJ2外,多数氧脂素仅通过质荷比推定,未完成精准分子鉴定;二是研究仅采用3种人细胞系和小鼠模型,结果难以覆盖所有细胞谱系与衰老诱导方式;三是未探究不同氧脂素的协同/拮抗作用,及潜在的其他调控通路。
展望后续研究方向:需精准鉴定衰老相关氧脂素的分子身份、解析其时空调控特征;验证二高-15d-PGJ2在人体体液中的检测可行性;深入探索氧脂素调控衰老的其他非经典通路,完善脂质-信号通路调控网络。
文献解读 | 麦角硫因通过CSE依赖的过硫化作用增强 cGPDH活性,延长老年动物的健康寿命
文献解读 | 分子伴侣介导的自噬导致 PLCG1 降解受损, 从而促进细胞衰老和椎间盘退变