衰老重编程通过协调的基因调控释放肿瘤免疫监视功能

该研究开发了靶向基因递送纳米颗粒TEPP,通过协同调控P16INK4a过表达与PD-L1敲低,重编程肿瘤衰老-免疫轴。TEPP借助uPAR靶向、TERT启动子及NLS-MTAS肽,实现肿瘤特异性基因递送与表达,增强肿瘤免疫原性并缓解免疫抑制。在三阴性乳腺癌、结直肠癌等多种肿瘤模型中,TEPP单药或联合免疫检查点抑制剂(如αCTLA-4)均展现出强效抑瘤、抗转移及防复发效果。该系统无明显系统毒性,为“冷肿瘤”的免疫治疗提供了可行策略。
Advanced Materials 2025年8月 IF26.8


1. 细胞衰亡可通过 SASP 招募免疫细胞发挥抗肿瘤作用,但免疫耐受及免疫抑制性TME会显著限制其治疗效果。
2. P16INK4a 能诱导肿瘤细胞衰老并增强免疫原性,却会通过上调或稳定 PD-L1,导致肿瘤发生免疫逃逸,削弱治疗效果。
3. 治疗诱导衰老易引发 T 细胞耗竭,现有联合治疗存在非特异性分布、肿瘤耐药等问题,临床应用受限。
4. 基因治疗可实现治疗分子持续表达,但缺乏精准靶向递送系统,现有纳米载体存在瞬时活性、易被巨噬细胞清除等不足。
5. uPAR 在衰老细胞上选择性高表达,为肿瘤特异性靶向递送提供了潜在靶点,成为解决现有治疗瓶颈的关键突破口。
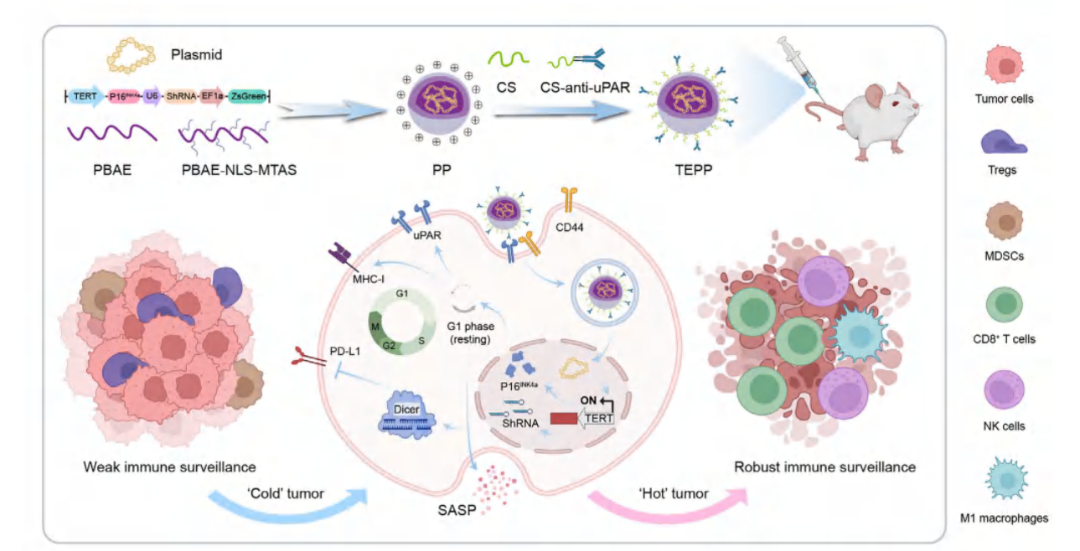
1. 明确科学问题与核心靶点:
针对细胞衰老疗法中 “P16INK4a 诱导肿瘤衰老但上调 PD-L1 导致免疫逃逸” 的矛盾,以及现有递送系统缺乏特异性、易被清除的缺陷,确定 “协同调控 P16INK4a(过表达)与 PD-L1(敲低)” 为核心治疗策略,同时发现 uPAR 在衰老肿瘤细胞上选择性高表达,将其作为靶向递送靶点。
2. 设计多功能靶向递送系统
构建 TEPP 纳米颗粒,以 PBAE 和 PBAE-NLS-MTAS 为核心载体(提升核递送效率),表面修饰 CS(结合肿瘤 CD44 受体)和 uPAR 抗体(精准靶向衰老肿瘤细胞),并搭载含 TERT 启动子的双功能质粒 pP16SP(实现肿瘤特异性基因表达)。
3. 分阶段验证功能与疗效
先通过体外实验验证 TEPP 的细胞摄取、质粒递送效率,以及对肿瘤细胞周期停滞、免疫原性提升的作用;再在体内皮下、肺转移、术后复发及自发肿瘤模型中,评估 TEPP 单药的抑瘤效果和生物安全性;最后探究 TEPP 与 αCTLA-4 免疫检查点阻断(ICB)的协同治疗潜力。
4. 解析作用机制与拓展应用
通过转录组、流式细胞术等分析 TEPP 对肿瘤微环境(TME)的重塑作用(激活 CD8+T 细胞、NK 细胞等免疫细胞,减少免疫抑制细胞);明确其通过 SASP 增强免疫原性、阻断 PD-L1 介导免疫耐受的双重机制,为 “冷肿瘤” 免疫治疗提供新方案。
1. P16INK4a 过表达通过衰老相关分泌表型(SASP)增强肿瘤免疫原性并促进免疫细胞浸润
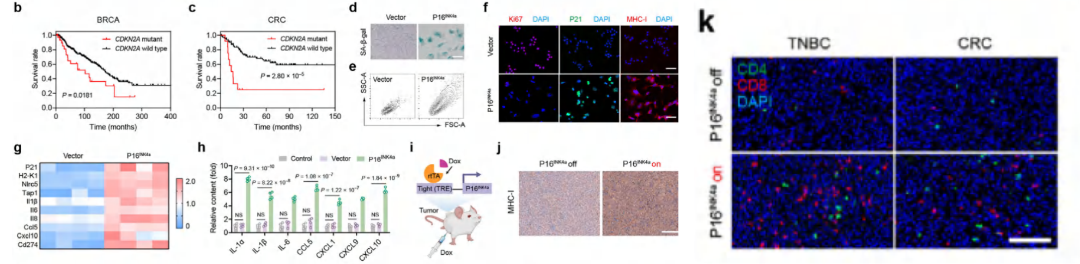
临床层面:CDKN2A 基因突变(编码 P16INK4a)或 P16INK4a 低表达,与乳腺癌、结直肠癌患者不良预后相关。
体外实验:P16INK4a 过表达可诱导肿瘤细胞衰老,提升 MHC-I 分子及抗原呈递相关基因表达,促进 SASP 相关促炎因子分泌。
体内效果:在小鼠肿瘤模型中,P16INK4a 过表达能升高肿瘤组织 MHC-I 水平,通过 SASP 的趋化作用,显著增加 CD4 + 和 CD8+ T 细胞在肿瘤部位的浸润。
2. P16INK4a 与 PD-L1 表达的协同调控有效克服免疫抑制
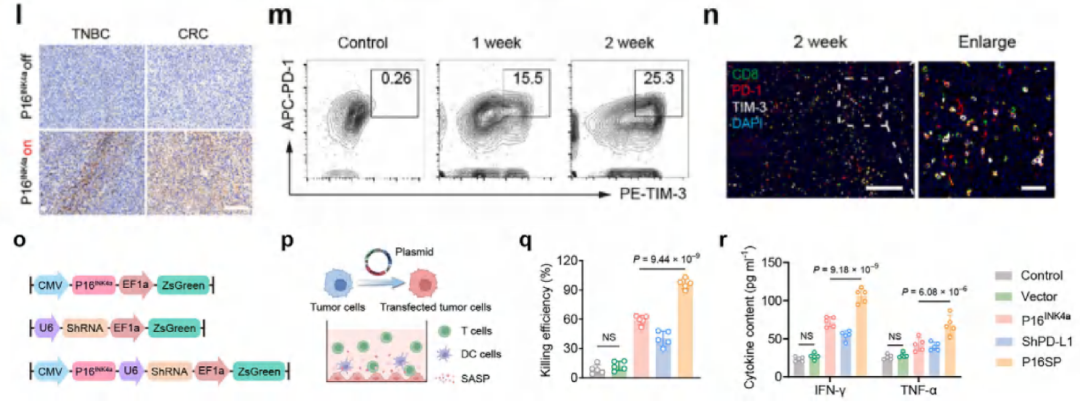
P16INK4a 过表达增强肿瘤免疫原性的同时,会上调 PD-L1 引发免疫耐受和 T 细胞耗竭。
构建双功能质粒 pP16SP,协同实现 P16INK4a 过表达与 PD-L1 敲低。
该质粒可显著提升免疫细胞对肿瘤细胞的杀伤能力,有效克服免疫抑制。
3. uPAR 靶向纳米颗粒 TEPP 的开发与表征
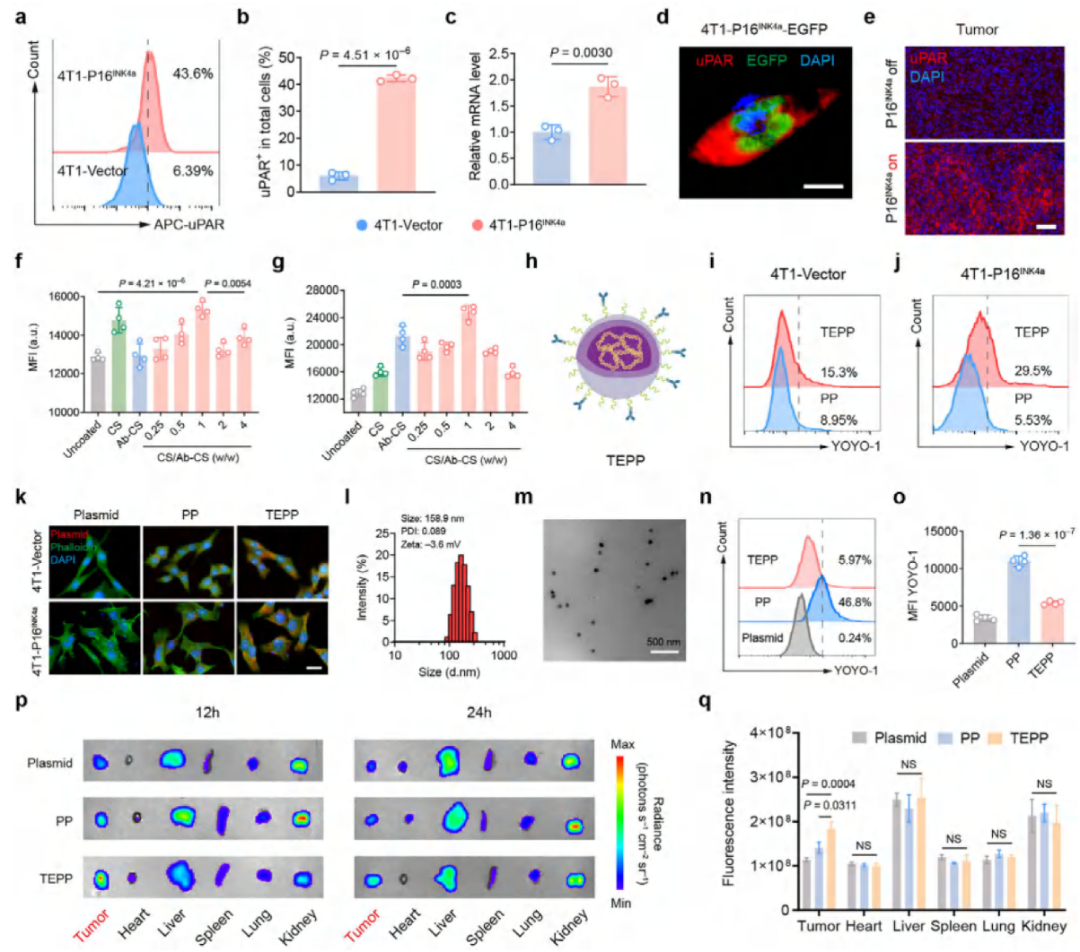
确认uPAR为肿瘤衰老特异性靶点,其表达随 P16INK4a 过表达显著上调。
构建TEPP纳米颗粒,以 PBAE-NLS-MTAS 为核心,修饰 CS 和 uPAR 抗体实现双靶向。
TEPP理化性质稳定,包封率高,可靶向富集于肿瘤组织,提升基因递送效率,且能减少巨噬细胞清除。
4. TEPP16SP 在体外诱导细胞周期停滞并激活免疫
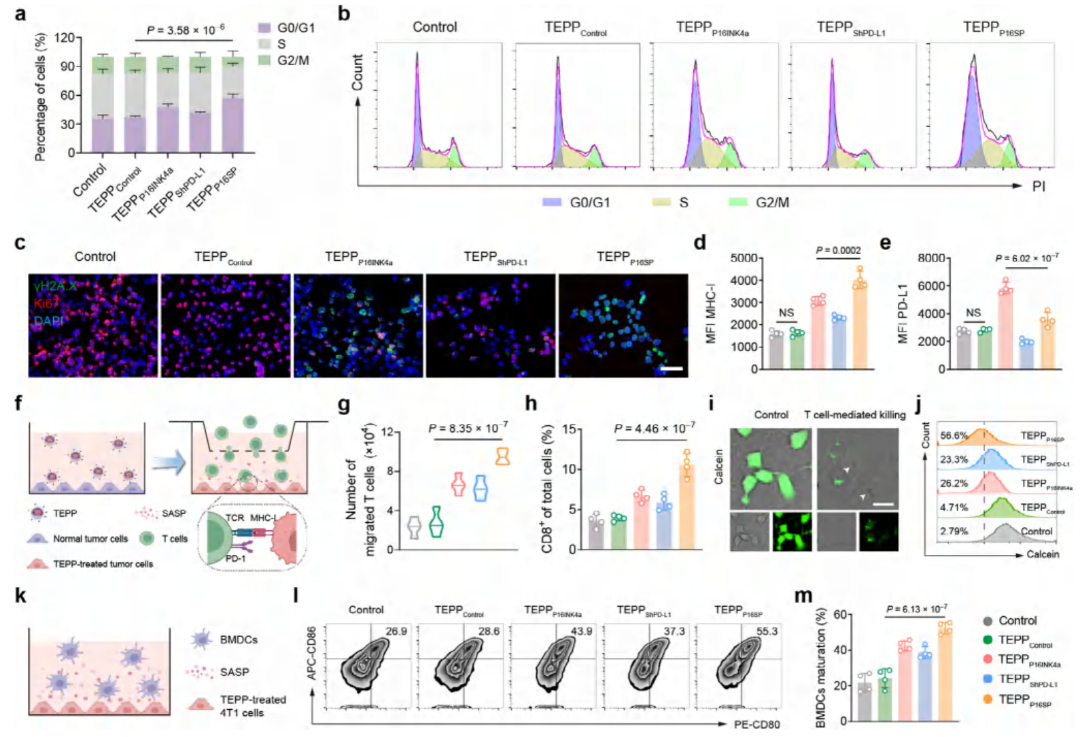
TEPP16SP 在体外可诱导肿瘤细胞 G1 期停滞并使其衰老。
能提升肿瘤细胞免疫原性(MHC-I↑、PD-L1↓)。
促进 T 细胞迁移与杀伤,激活 BMDC,增强抗肿瘤免疫应答。
5. TEPP16SP 的体内肿瘤特异性表达及抗肿瘤疗效
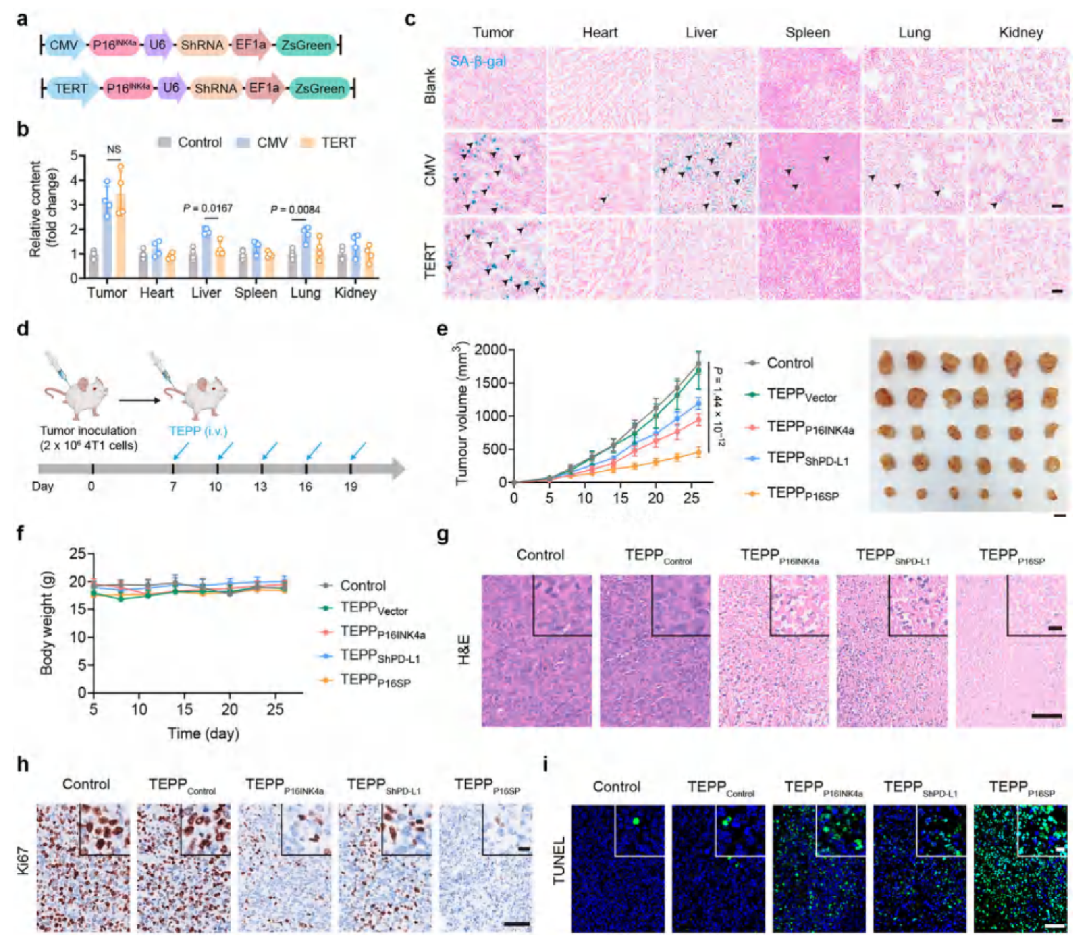
采用 TERT 启动子,实现 TEPP16SP 在肿瘤组织的特异性表达,降低脱靶效应。
在 TNBC 模型中展现强效抑瘤作用,抑制率显著优于单一基因调控策略。
3.治疗无明显全身毒性,生物安全性良好。
6.TEPP16SP 重塑免疫抑制性肿瘤微环境(TME)
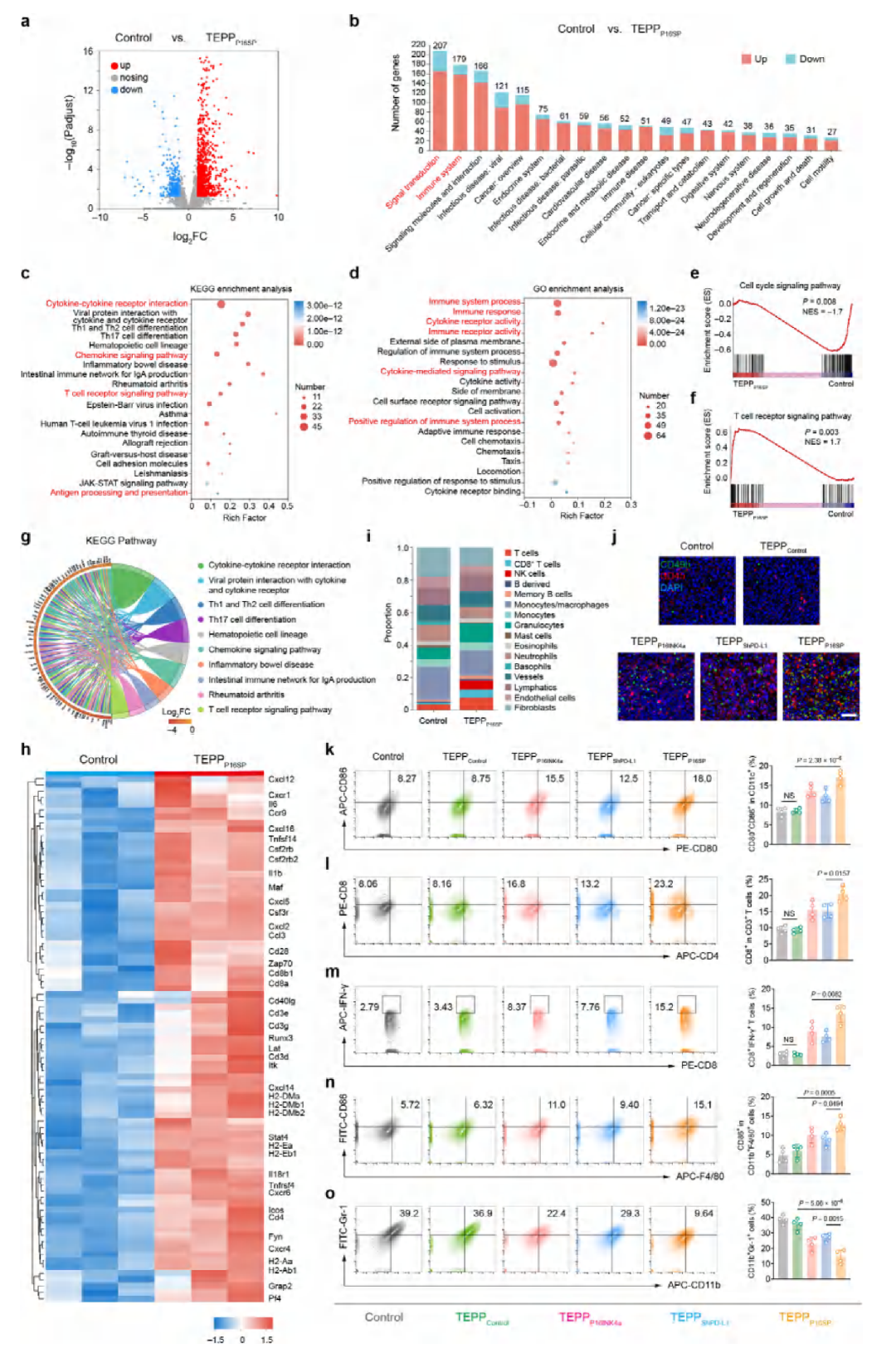
TEPP16SP 可显著改变肿瘤组织转录组,激活免疫相关通路。
增加 NK 细胞、CD8+T 细胞等效应免疫细胞浸润,提升 DC 成熟度和 M1 巨噬细胞比例。
减少免疫抑制性细胞(如 MDSCs),有效重塑免疫抑制性 TME,增强抗肿瘤免疫。
7. TEPP16SP 联合免疫检查点阻断(ICB)的抗肿瘤效应
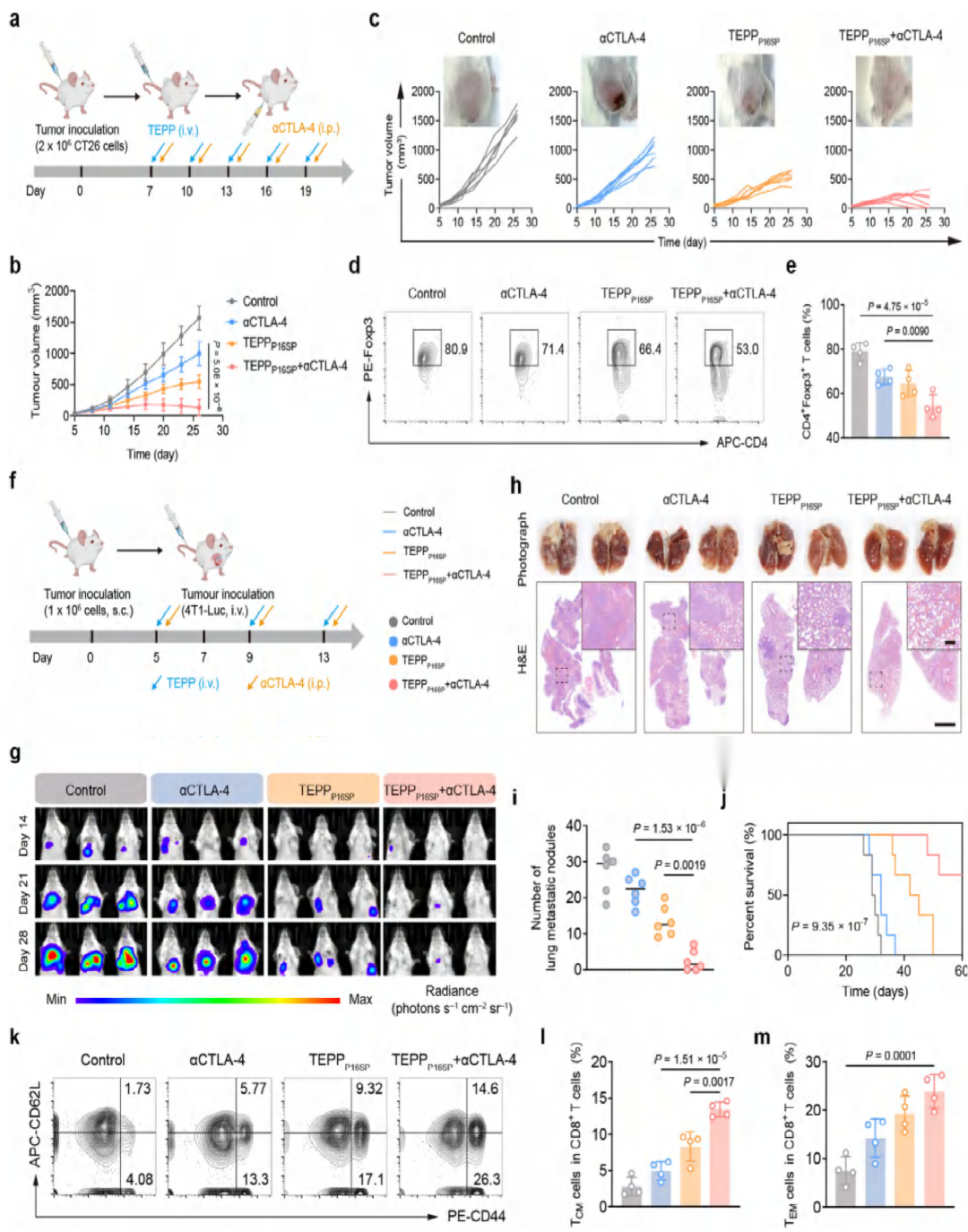
TEPP16SP 与 αCTLA-4 联合治疗,在 CRC、TNBC 转移及复发等多种模型中均显著提升抗肿瘤效果。
联合治疗可减少肿瘤微环境中 Tregs,增加记忆 T 细胞,强化免疫记忆与效应 T 细胞浸润。
能有效抑制肿瘤原发、转移及术后复发,显著延长荷瘤小鼠生存期。
TEPP16SP通过协同调控P16INK4a过表达与PD-L1敲低,重编程肿瘤衰老-免疫轴,强化抗肿瘤免疫。该纳米系统以uPAR为靶向靶点,结合 TERT 启动子与NLS-MTAS肽,实现肿瘤特异性高效基因递送。
其单药可有效抑瘤,联合免疫检查点阻断疗法能显著提升多种肿瘤模型(原发、转移、复发)的治疗效果,为免疫 “冷肿瘤” 提供新策略。
未来需进一步拓展靶点与肿瘤类型,优化治疗安全性与适用性。
首创 “P16INK4a 过表达 + PD-L1 敲低” 协同调控,破解衰老诱导伴随的免疫逃逸难题。
构建 uPAR 靶向的 TEPP 纳米系统,实现肿瘤特异性、高效基因递送。
联合 ICB 拓展至转移、复发等多肿瘤场景,强化免疫记忆,提升治疗适用性。