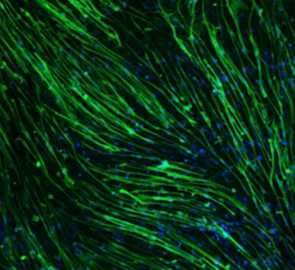
麦角硫因通过CSE依赖的过硫化作用增强 cGPDH活性,延长老年动物的健康寿命

Petrovic等人证实,麦角硫因可作为γ-胱硫醚酶的替代底物,进而增加蛋白质硫化修饰水平。cGPDH经硫化修饰后其活性得到增强,最终导致NAD+水平升高。用麦角硫因处理老年动物,可改善其健康寿命和体能表现。
Cell Metabolism 2025年1月21日 IF30.9
衰老不可避免地导致健康寿命缩短和生理功能衰退,给全球医疗系统带来巨大压力,因此寻找能缓解年龄相关损伤、提升整体健康水平的解决方案,成为近年来的研究热点。其中,挖掘具有治疗潜力的天然化合物是重要探索方向。
ET 是一种天然存在的膳食硫醇 / 硫酮化合物,主要来源于真菌和放线菌等饮食来源,可通过 OCTN1(Slc22a4)转运体在细胞内大量积累,该转运体在哺乳动物和秀丽隐杆线虫中均存在。
早期研究认为 ET 的有益作用源于抗氧化活性,但后续发现其还原电位较低,对细胞内多数氧化剂(如过氧化氢)无反应,说明抗氧化并非其核心作用机制。
已有研究提示 ET 的潜在价值:可促进雄性小鼠长寿和健康衰老;血液中 ET 水平与衰老进程、帕金森病、阿尔茨海默病等衰老相关疾病呈负相关;对 β- 淀粉样蛋白诱导的神经损伤、缺血再灌注损伤具有保护作用。
尽管 ET 的有益效应已被初步观察,但它对老年动物健康寿命的具体影响(如体能、组织功能等),以及驱动这些效应的分子机制尚未明确,这为本文的研究提供了核心切入点。
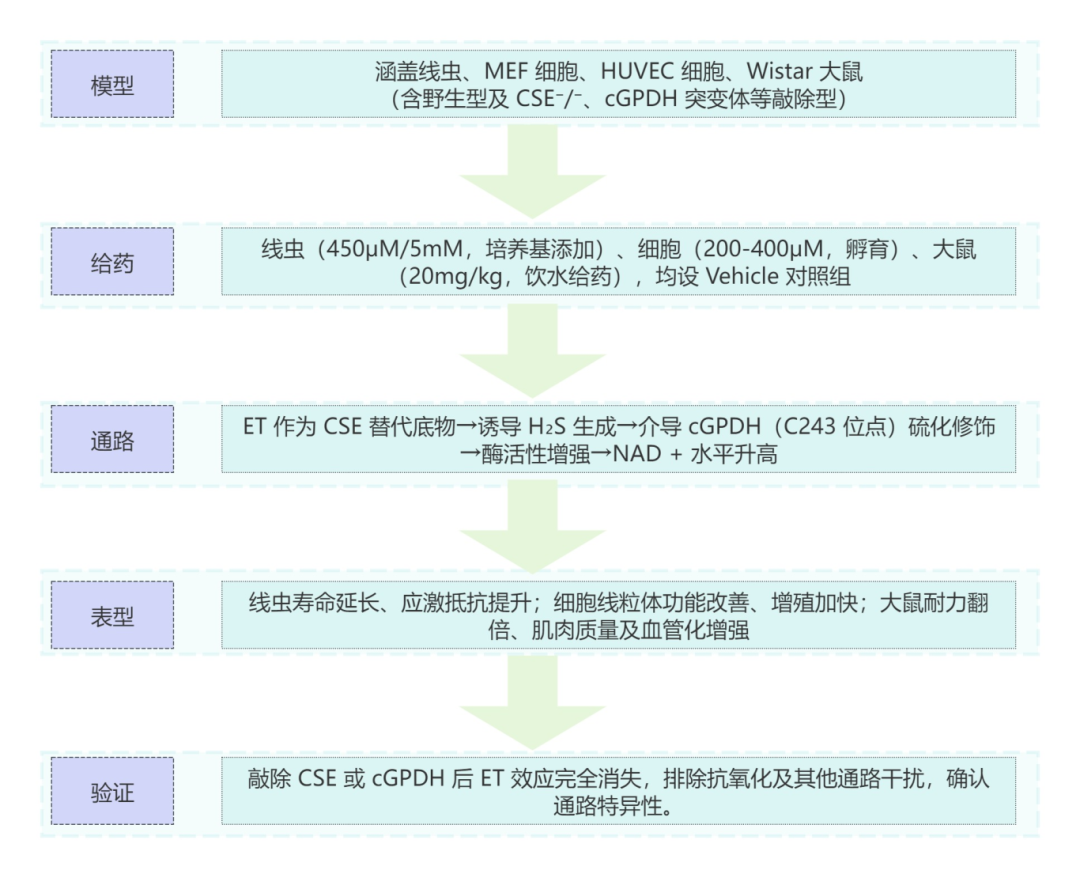 本研究探究了 ET 对老年动物健康寿命的影响,结果显示,ET 可延长秀丽隐杆线虫的寿命并提升其运动能力,同时增强其应激抵抗力且降低年龄相关生物标志物水平。
本研究探究了 ET 对老年动物健康寿命的影响,结果显示,ET 可延长秀丽隐杆线虫的寿命并提升其运动能力,同时增强其应激抵抗力且降低年龄相关生物标志物水平。
在老年大鼠中,ET 给药可提高运动耐力、增加肌肉质量并促进血管生成,同时伴随肌肉组织中烟酰胺腺嘌呤二核苷酸(NAD+)水平升高。
机制上,ET 可作为 γ- 胱硫醚酶(CSE)的替代底物,促进硫化氢(H₂S)生成,进而使超过 300 种蛋白质靶点发生硫化修饰。其中,胞质甘油 - 3 - 磷酸脱氢酶(cGPDH)经硫化修饰激活,是 ET 诱导 NAD + 水平升高的主要原因。
在缺失 CSE 或 cGPDH 的模型中,ET 的上述效应完全消失,这凸显了 H₂S 信号通路和蛋白质硫化修饰的关键作用。
这些发现阐明了 ET 的多方面作用,为其用于应对年龄相关的肌肉衰退和代谢紊乱提供了新的见解和治疗潜力。
1. 寿命与健康 span 改善
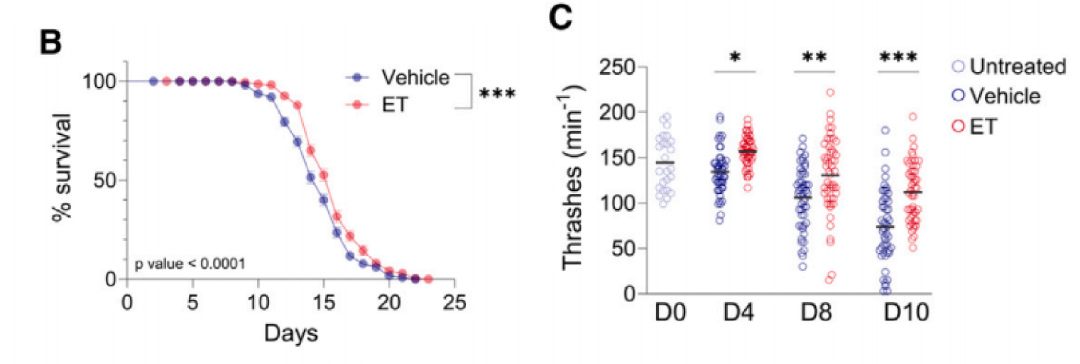
ET(5 mM/450 μM)可显著延长野生型线虫中位寿命(20%±2%/6.8%±0.3%)和最大寿命,且能维持老年线虫(D10)的运动能力(摆尾频率),改善健康 span。
2. 应激抵抗与衰老标志物降
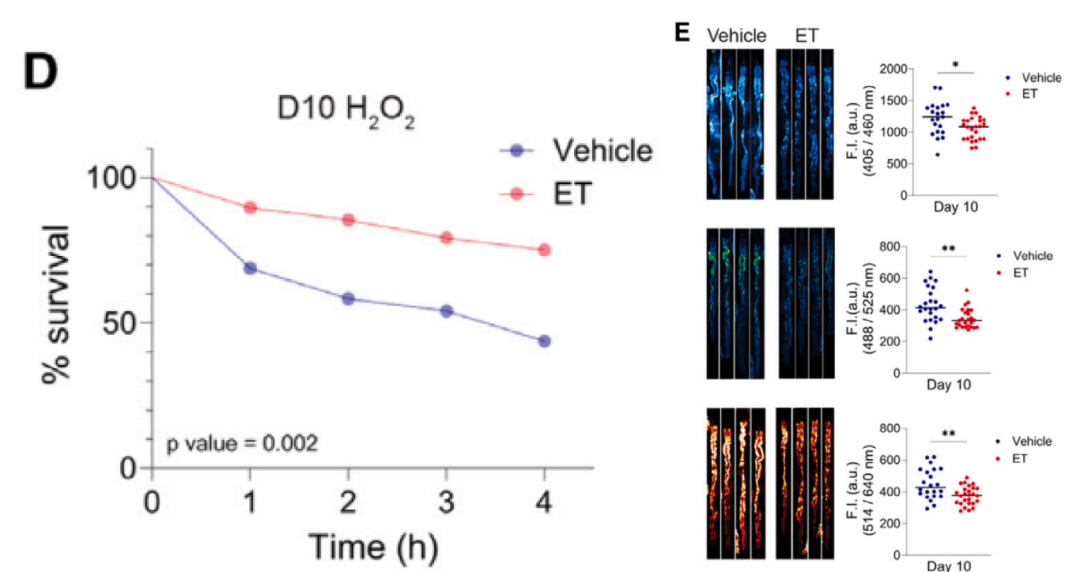
T 增强线虫对 H₂O₂、百草枯、砷酸盐、热休克的抵抗力,降低肠道脂褐素 autofluorescence 和脂质积累,不影响脂质过氧化标志物(4-HNE)。
3. 线粒体形态保护
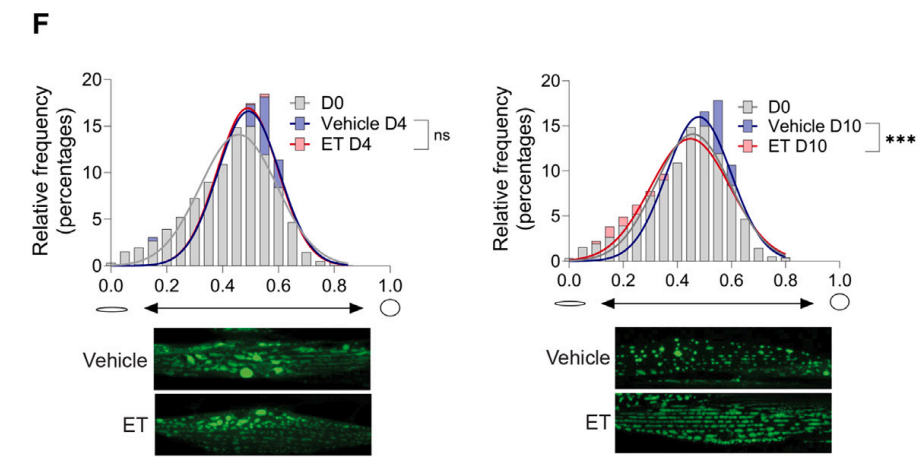
ET 处理可减少老年线虫线粒体碎片化,维持线粒体伸长形态,与运动能力改善相关。
4. 转录组 / 蛋白质组特征
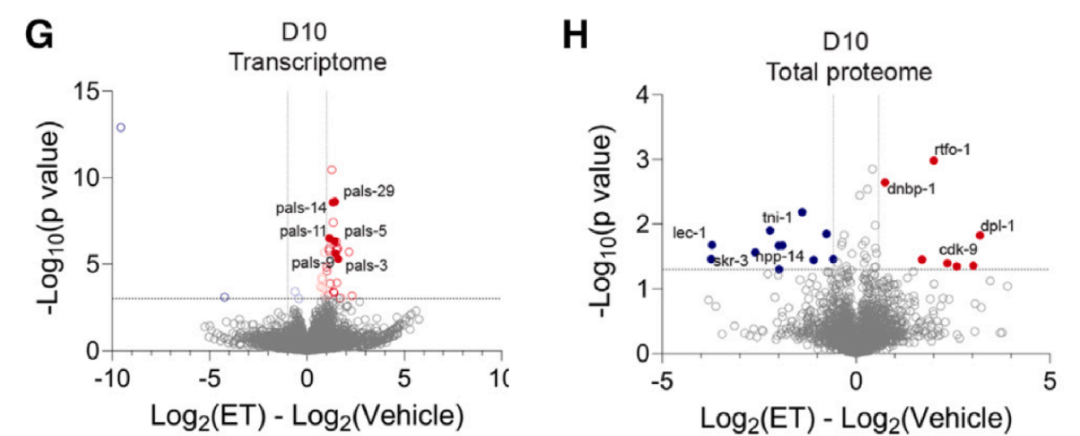
ET 对转录组和总蛋白质组调控靶点极少且无重叠,排除转录 / 翻译调控。
5. 蛋白质硫化修饰激活
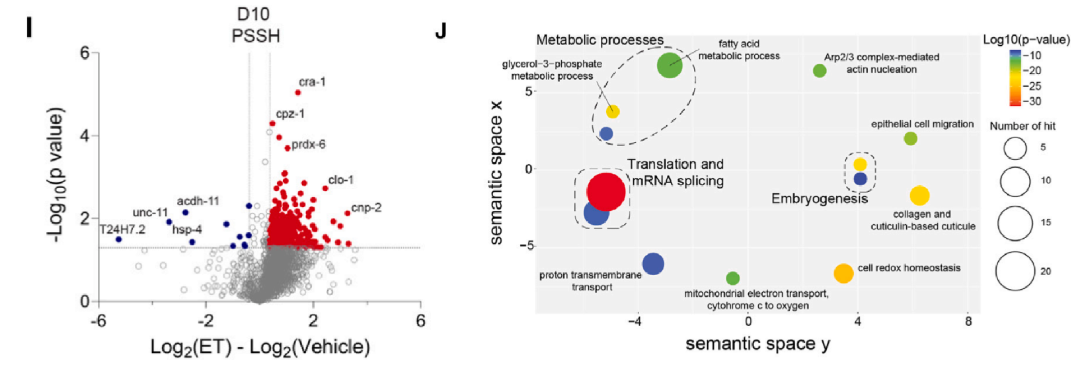
ET 显著提高 > 300 种蛋白的硫化修饰(PSSH)水平,富集于线粒体 ATP 合成酶复合体、甘油 - 3 - 磷酸代谢等通路。
1.CSE 是 ET 关键结合靶点
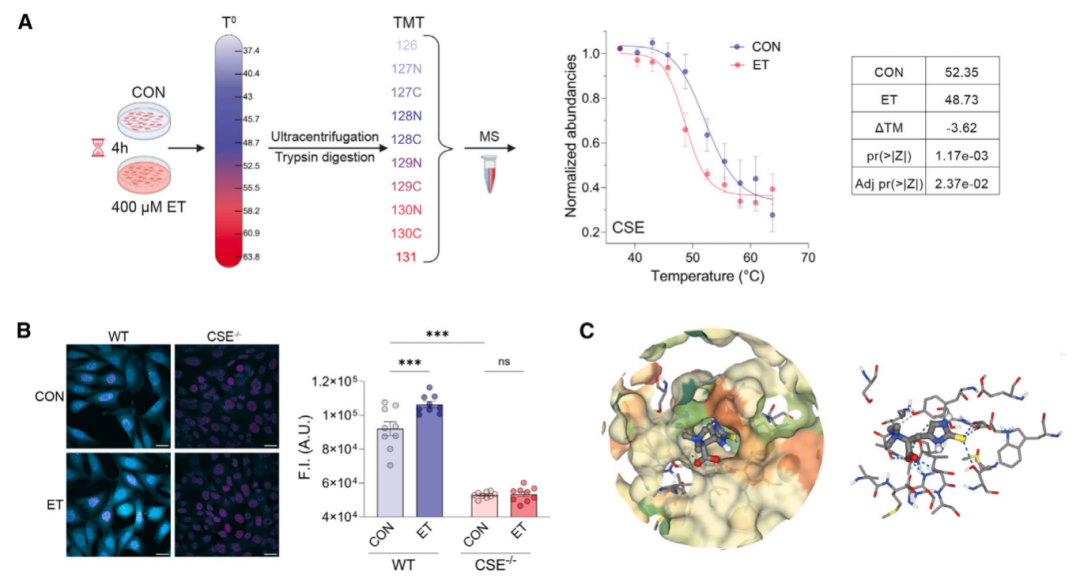
热蛋白质组分析(TPP)、等温剂量反应实验证实 ET 与 CSE 结合,分子对接显示 ET 结合于 CSE 活性位点。
2. ET 作为 CSE 替代底物
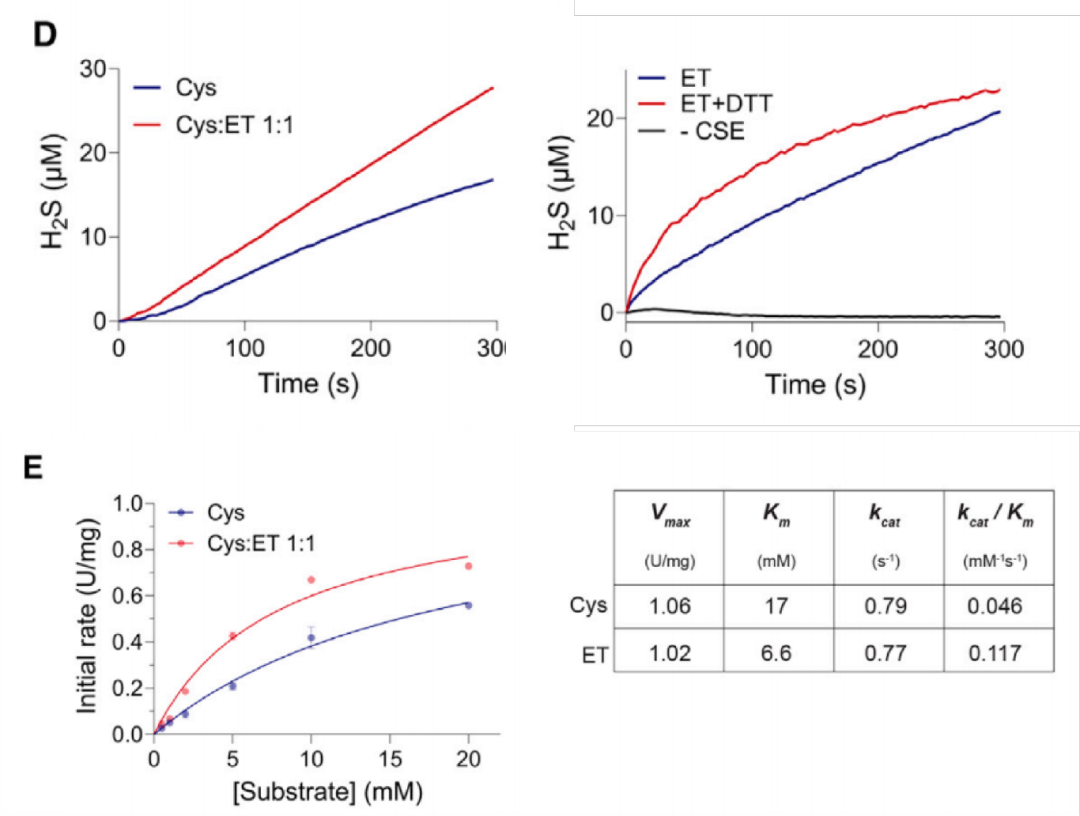
重组 CSE 利用 ET 生成 H₂S,不抑制半胱氨酸介导的 H₂S 生成,ET 的 Km 低于半胱氨酸。
3. CSE 催化 ET 脱硫生成 hercynine
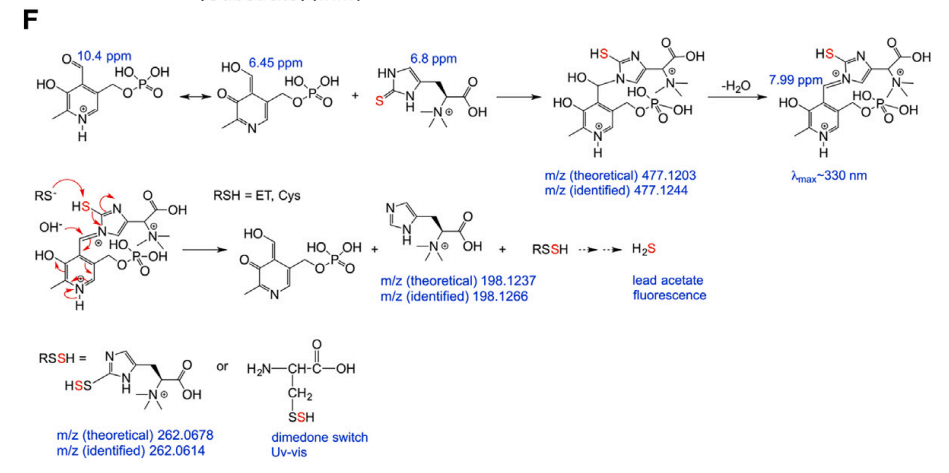
依赖 PLP 介导,经 Schiff 碱中间体生成 hercynine,中间产物含 ET 过硫化物和半胱氨酸过硫化物。
4. CSE 依赖性验证和细胞内代谢影响
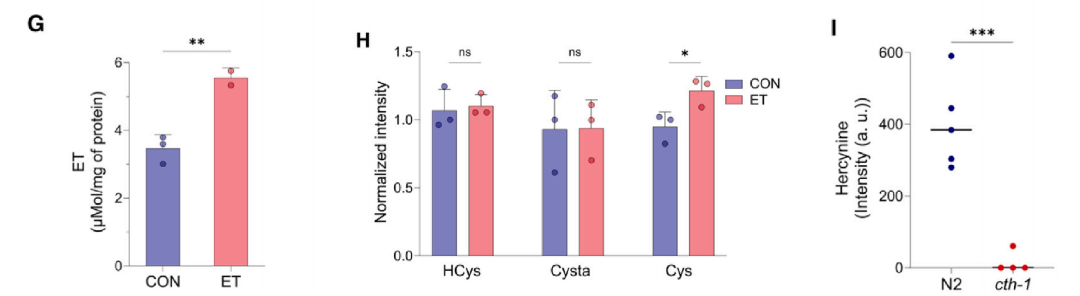
CSE⁻/⁻细胞 /cth-1 突变线虫中,ET 无法诱导 H₂S 生成、蛋白质硫化修饰及 hercynine 合成。
ET 处理提高 MEF 细胞内半胱氨酸水平,不影响同型半胱氨酸和胱硫醚。
细胞水平功能验证结果
1. 线粒体功能改善
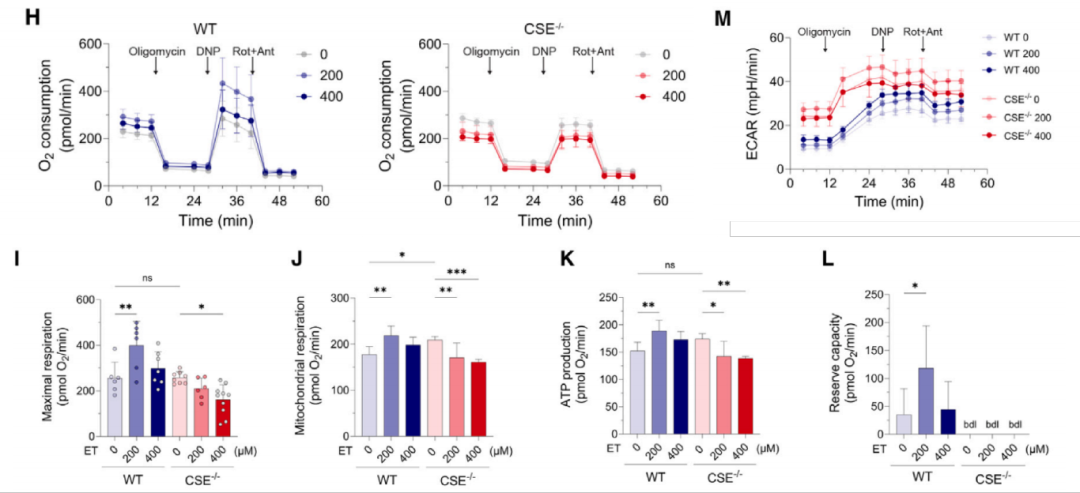
ET 提高 WT MEF 细胞最大呼吸、线粒体呼吸、ATP 产量和储备呼吸容量(RRC),CSE⁻/⁻细胞中效应消失,ECAR 无变化(排除糖酵解调控)。
2. 细胞增殖与血管生成增强
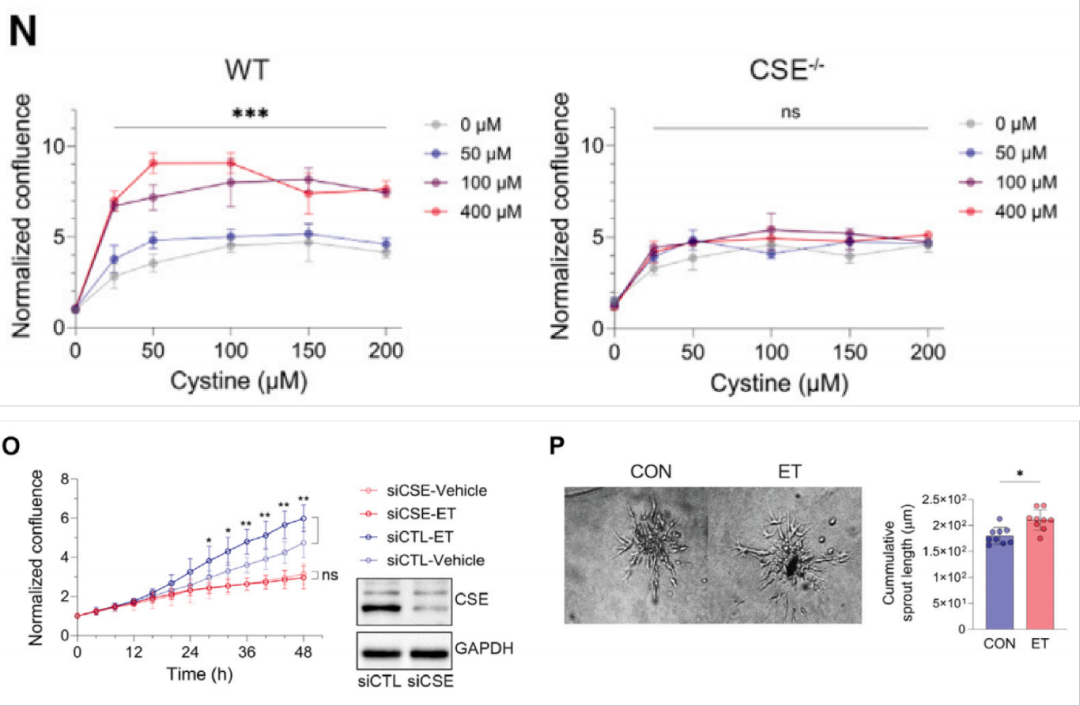
ET 浓度依赖性促进 MEF 和 HUVEC 增殖,提高 HUVEC 成芽能力,沉默 CSE 后效应消失,依赖细胞周期 G2/M 期激活,与 mTOR 通路无关。
大鼠体内验证结果
1. 体能与肌肉健康改善、代谢与 NAD⁺水平改善
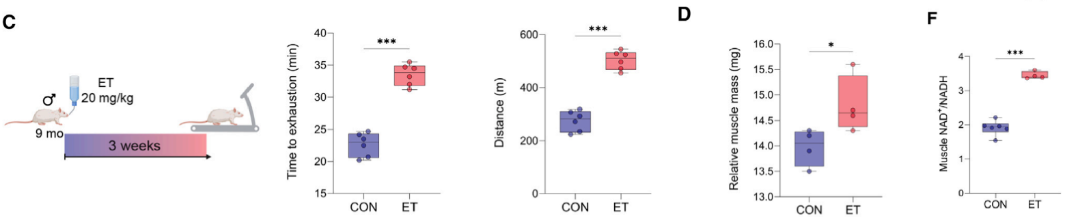
9 月龄大鼠 ET(20 mg/kg,3 周)处理后,跑步机力竭时间和距离翻倍,腓肠肌质量增加,运动后乳酸水平降低。
肌肉组织 NAD⁺/NADH 比值升高,NADP⁺/NADPH 平衡偏向还原态,丙酮酸、草酰乙酸水平无变化。
2. 血管化与肌肉干细胞增多
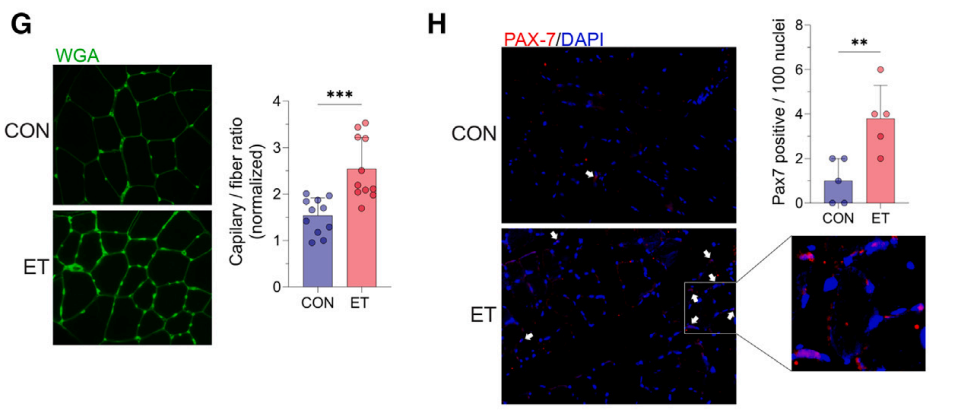
肌肉纤维周围血管数量增加,VEGFR 蛋白水平升高,肌肉干细胞(PAX-7⁺)数量增多,线粒体活性增强。
cGPDH 的核心靶标作用结果
1.cGPDH 硫化修饰与活性激活
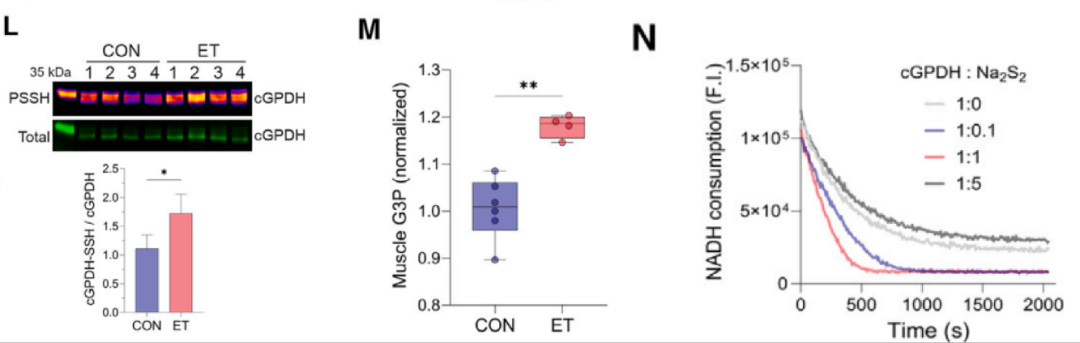
ET 诱导线虫 GPDH2、大鼠肌肉 cGPDH 的 C243 位点硫化修饰,体外 Na₂S₂处理使 cGPDH 活性翻倍。
2. 代谢通路关联
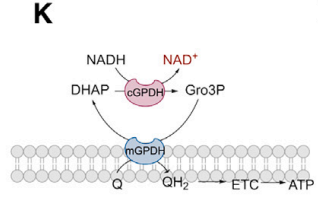
cGPDH 激活通过甘油 - 3 - 磷酸穿梭促进胞质 NADH 再生为 NAD⁺,衔接 H₂S 信号与 NAD⁺代谢。
3. 肌肉组织 cGPDH 活性
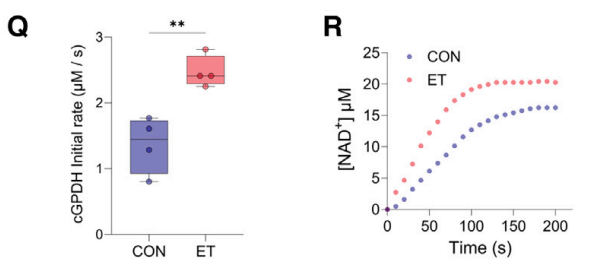
ET 诱导线虫 GPDH2、大鼠肌肉 cGPDH 的 C243 位点硫化修饰,体外 Na₂S₂处理使 cGPDH 活性翻倍。
1. 核心机制确立:ET的有益效应依赖“ET-CSE-H₂S-cGPDH-NAD⁺”通路,CSE是关键介导者,H₂S信号与蛋白质硫化修饰不可或缺。
2. 认知纠正与创新:ET并非通过直接抗氧化作用起效,而是以翻译后修饰(硫化)调控代谢通路;cGPDH作为核心靶标,连接H₂S信号与NAD⁺代谢,为相关疾病干预提供新思路。
3. 与已有研究的优势:ET对老年动物健康改善效应堪比甚至优于NAD⁺前体(NR、NMN),且短期补充即起效;呼应H₂S已知的长寿、血管保护作用,完善其分子机制。
4. 应用潜力:可用于干预年龄相关肌肉衰退和代谢紊乱,短期使用或能提升运动表现;天然膳食来源且可通过生物工程扩大产量,转化可行性高。
5. 局限性:老年个体CSE表达下降可能削弱ET效果;人类CSE突变者或无法获益;需警惕过量补充导致的H₂S毒性风险。
6. 未来方向:探索ET在人类相关疾病中的临床效果;开发ET与CSE激活剂的联合方案;优化ET膳食来源与安全剂量。