Ti₃C₂/锌铝层状双氢氧化物纳米平台增强的光热 - 免疫调节水凝胶用于根除耐甲氧西林金黄色葡萄球菌并促进糖尿病创面愈合

◆MRSA 感染与糖尿病创面治疗的临床困境
耐甲氧西林金黄色葡萄球菌(MRSA)具有高侵袭性、高死亡率及广泛的多重耐药性,其引发的慢性皮肤损伤易进展为骨髓炎、败血症等严重组织侵袭性疾病。糖尿病患者的 MRSA 感染创面尤为难治,常表现为持续炎症、血管生成障碍及组织再生延迟,核心原因包括 MRSA 形成的顽固生物膜、对抗生素的多重耐药性,以及传统抗生素难以在创面局部维持有效浓度,导致临床干预效果有限。
◆传统治疗方案的局限性
抗生素治疗:广谱抗生素因耐药性加剧、组织靶向性不足及毒副作用明显,应用价值日益受限,无法有效解决 MRSA 感染的顽固性问题。
新兴治疗手段:噬菌体疗法、刺激响应型生物材料等新兴策略,仍存在抗耐药能力不足、靶向效率低、抗菌机制单一等缺陷,难以实现感染清除与创面修复的协同效果。
◆天然 NETs 的治疗潜力与固有缺陷
中性粒细胞胞外诱捕网(NETs)通过 DNA 网状结构物理捕获细菌,并借助活性氧(ROS)、组蛋白等发挥直接杀菌作用,同时可招募免疫细胞促进 MRSA 清除,在慢性创面治疗中展现出显著潜力。但 MRSA 已进化出多种逃逸机制,包括分泌核酸酶降解 NETs 的 DNA 支架、产生葡萄球菌黄素淬灭氧化应激、抑制 NETs 形成及修饰表面结构降低亲和力等,导致天然 NETs 的治疗效果受限,难以破解慢性感染难题。
◆研究需求与技术突破口
针对 MRSA 耐药性、糖尿病创面免疫微环境紊乱(如免疫衰老)及现有治疗手段的不足,亟需开发兼具精准靶向、高效抗菌及免疫调节功能的新型治疗策略。基于 2D 材料的仿生设计与光热治疗技术的结合,为模拟 NETs 抗菌防御功能、克服其固有缺陷提供了可行路径,有望实现 MRSA 感染清除与糖尿病创面修复的协同治疗。
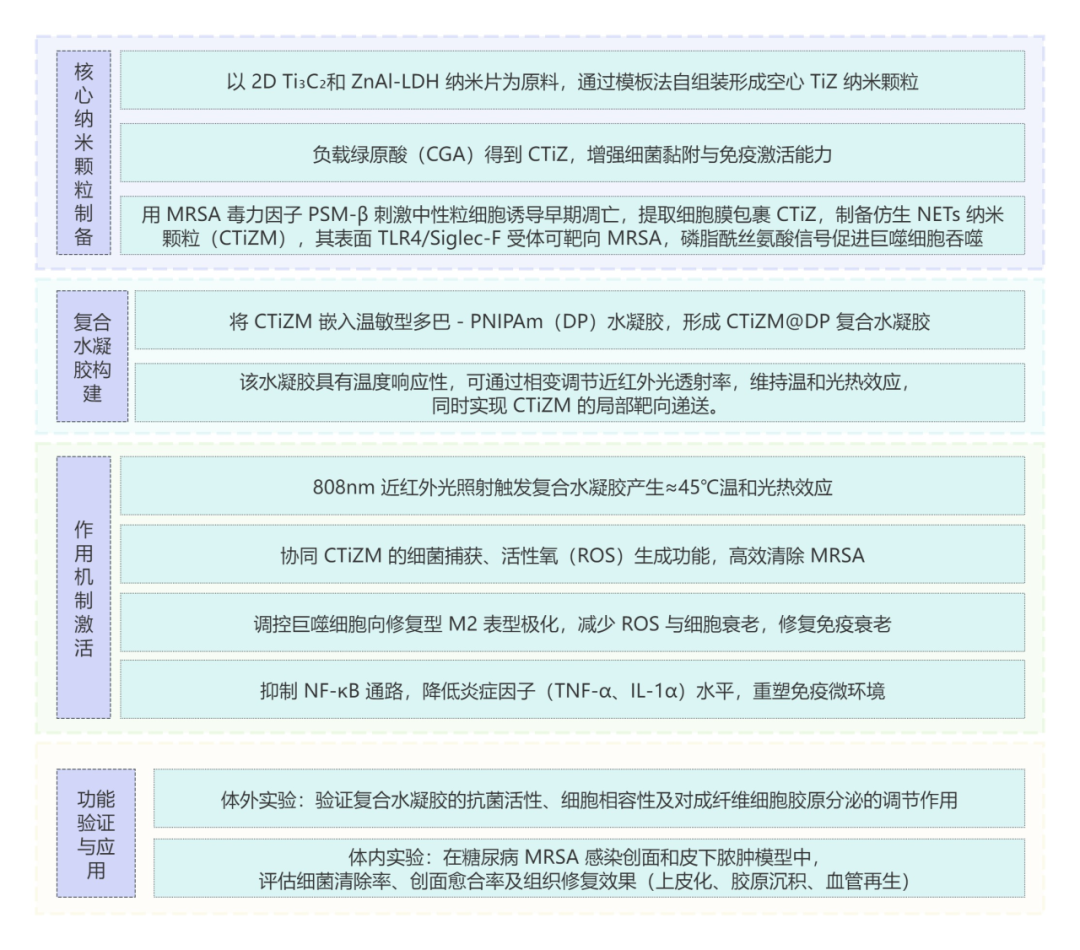
本文针对MRSA感染糖尿病慢性创面的治疗难题,借鉴天然NETs的抗菌与免疫调节功能,设计了CTiZM@DP复合水凝胶:以Ti3C2/ZnAl-LDH为基础构建空心纳米颗粒并负载绿原酸,包裹凋亡中性粒细胞膜形成仿生NETs(CTiZM),嵌入温敏水凝胶后,经近红外光触发温和光热效应,协同实现MRSA清除、巨噬细胞M2极化及免疫衰老修复,最终促进创面愈合。
1
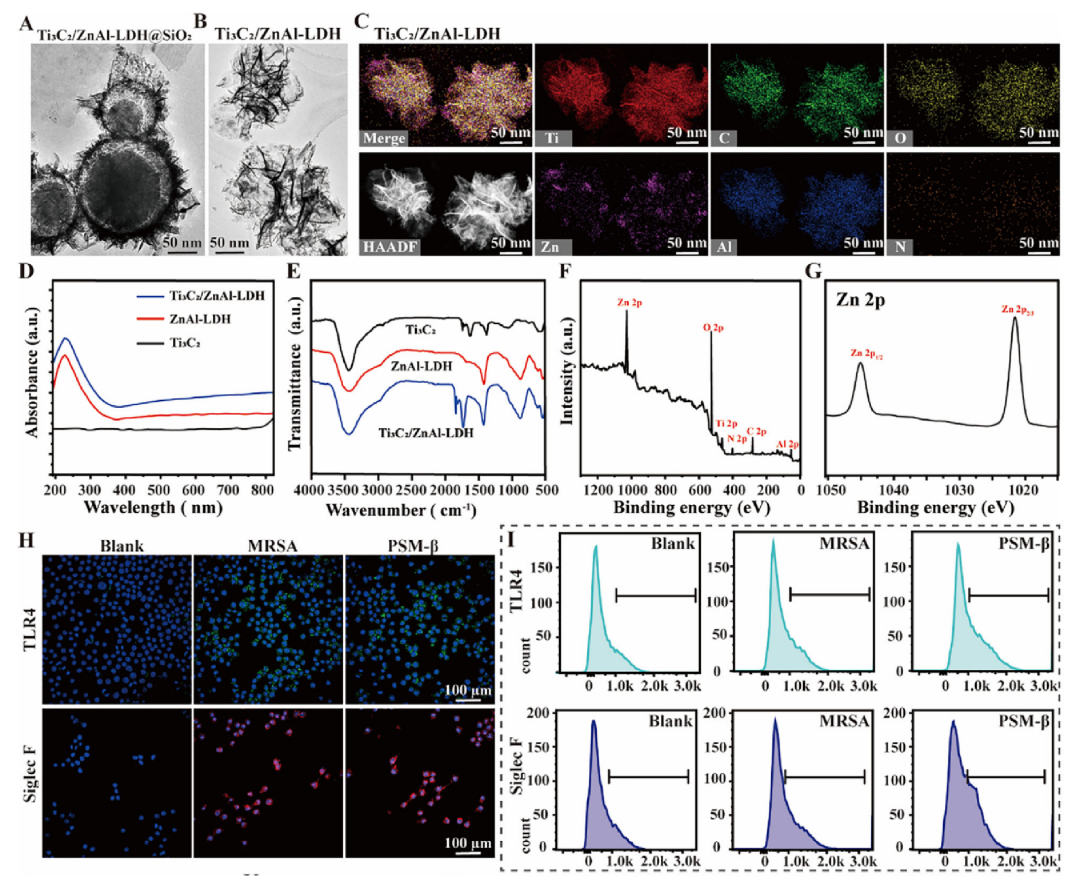
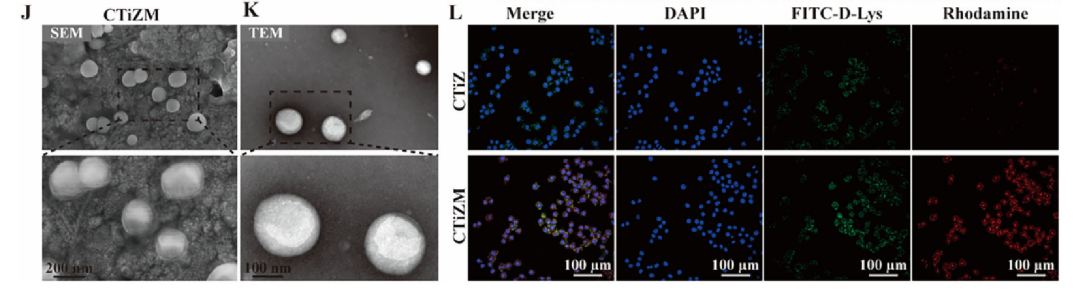
CTiZM 仿生 NETs 纳米颗粒的制备与表征
2
CTiZM@DP 光敏水凝胶的制备、体外生物活性及抗菌性能评估
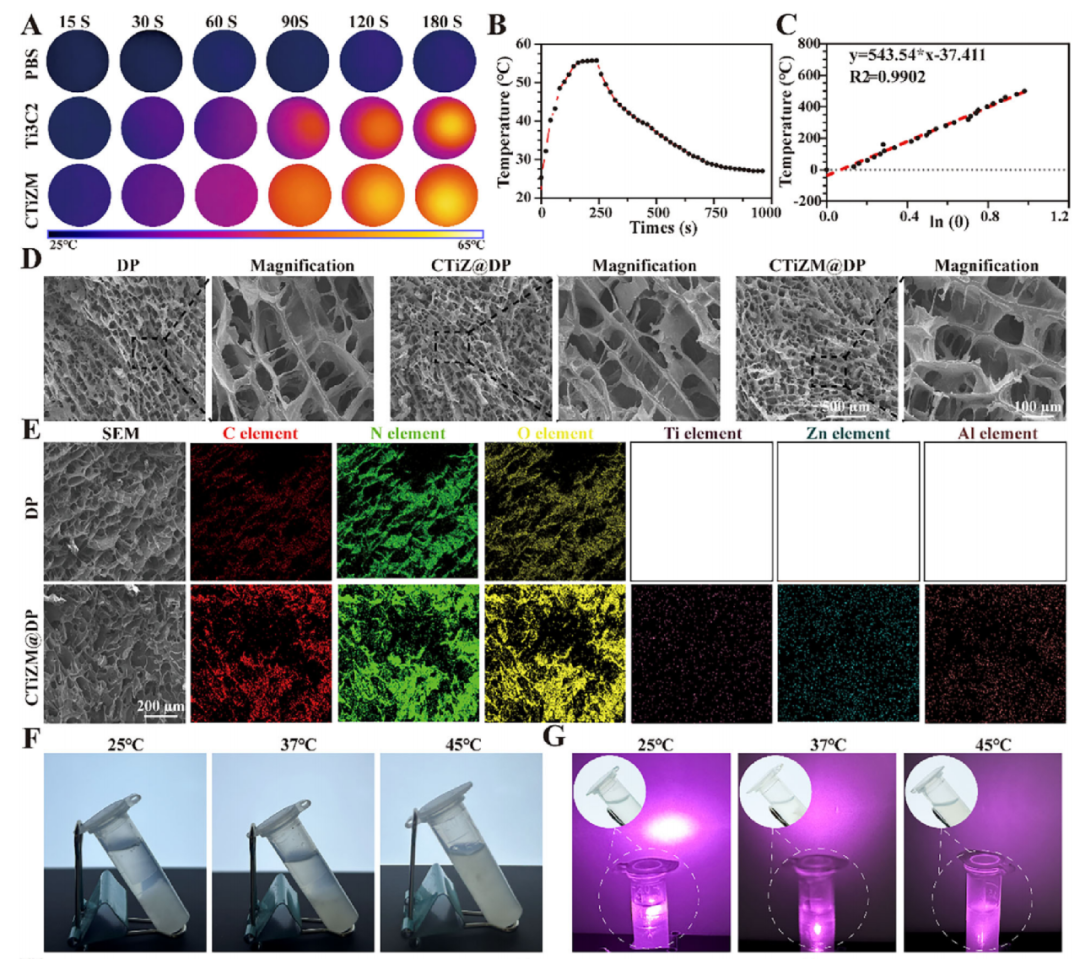
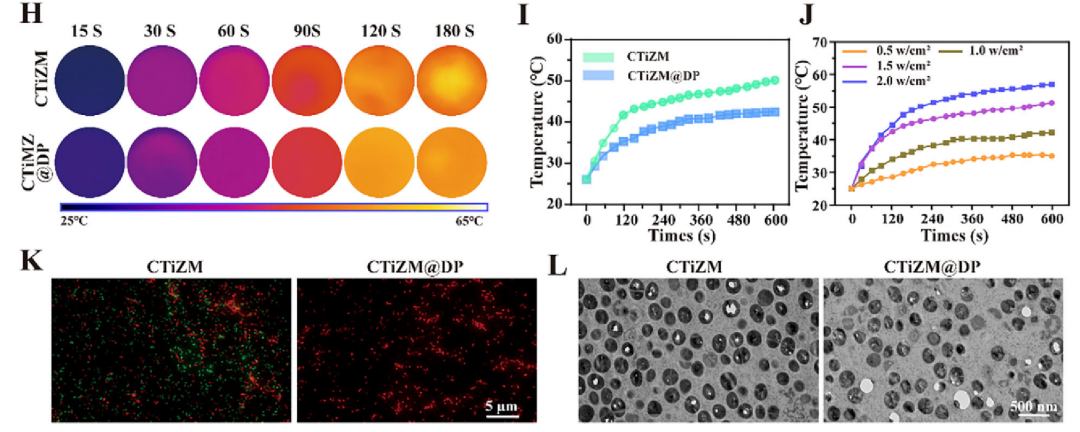
3
CTiZM@DP 水凝胶靶向衰老巨噬细胞,修复免疫衰老并重塑免疫微环境
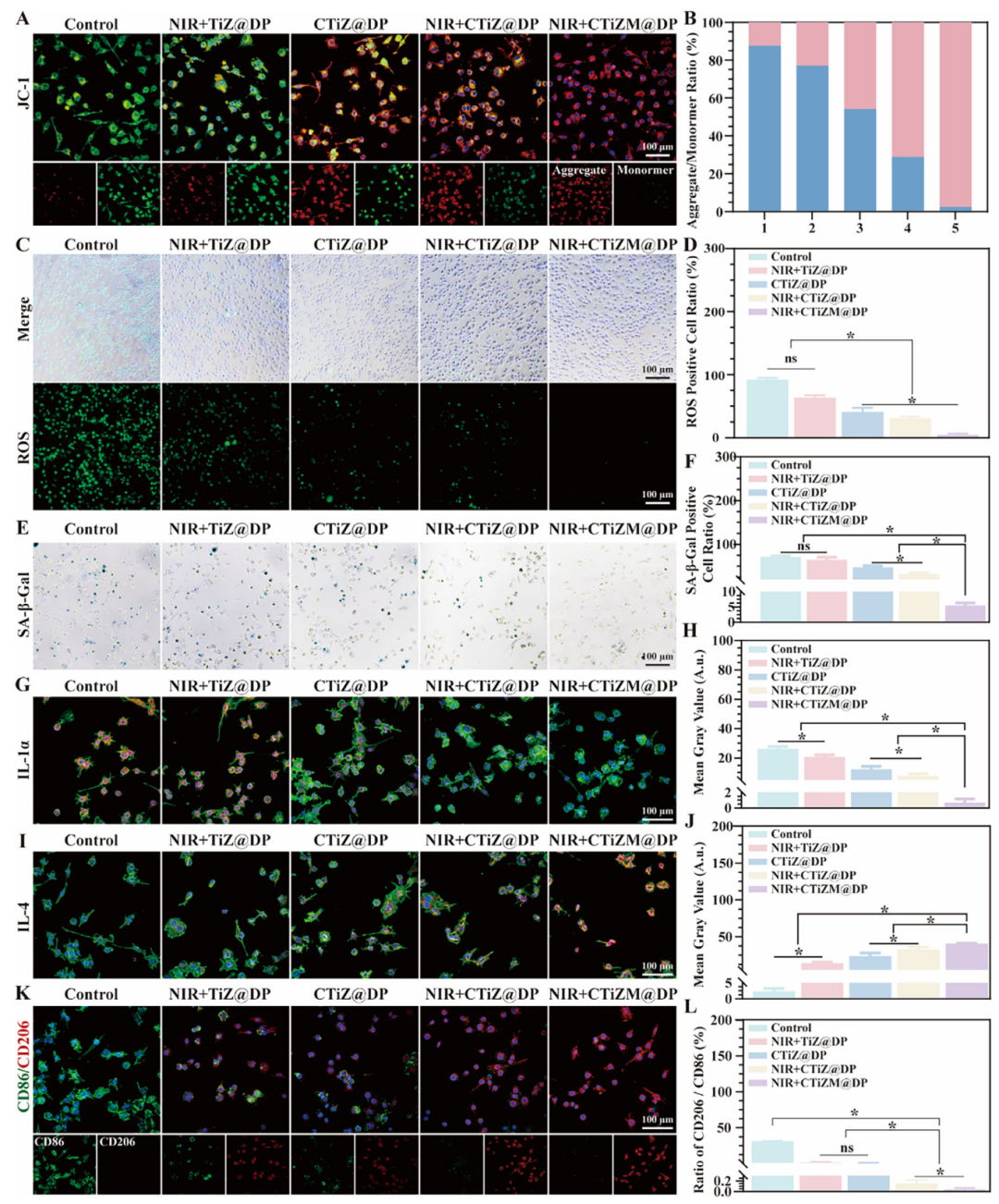
4
CTiZM@DP 光热水凝胶通过调控成纤维细胞表型重塑再生微环境
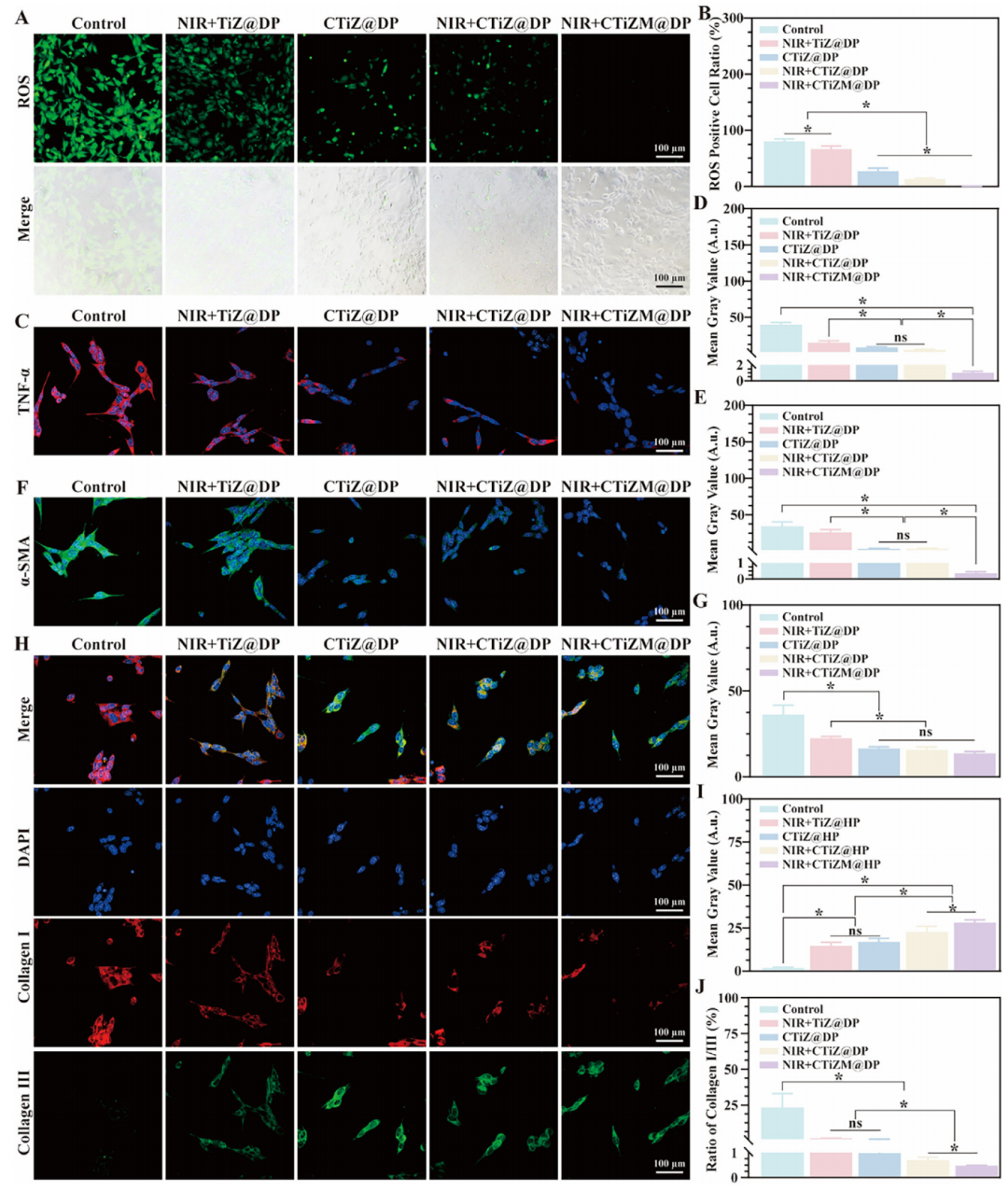
5
CTiZM@DP 光敏水凝胶的体内抗菌与促修复效应
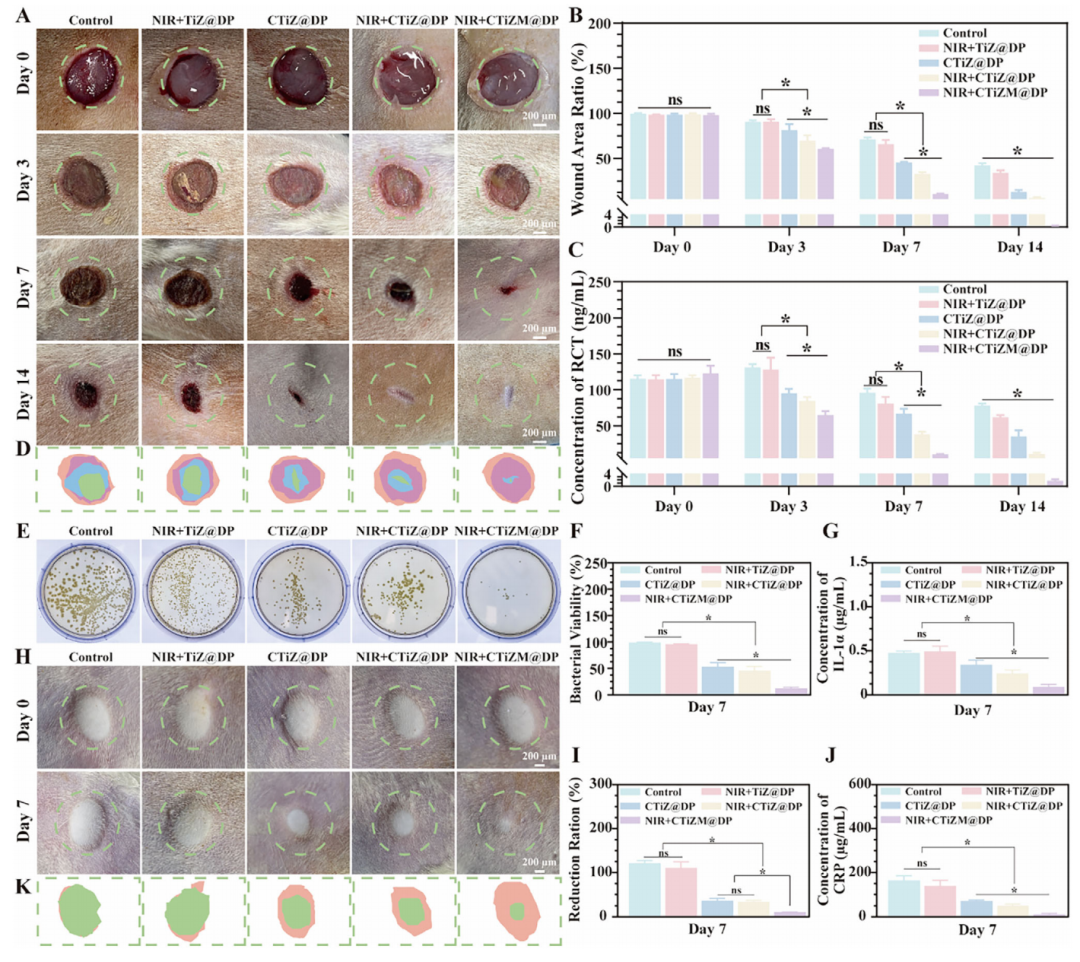
6
CTiZM@DP 光热凝胶促进创面上皮化与胶原沉积
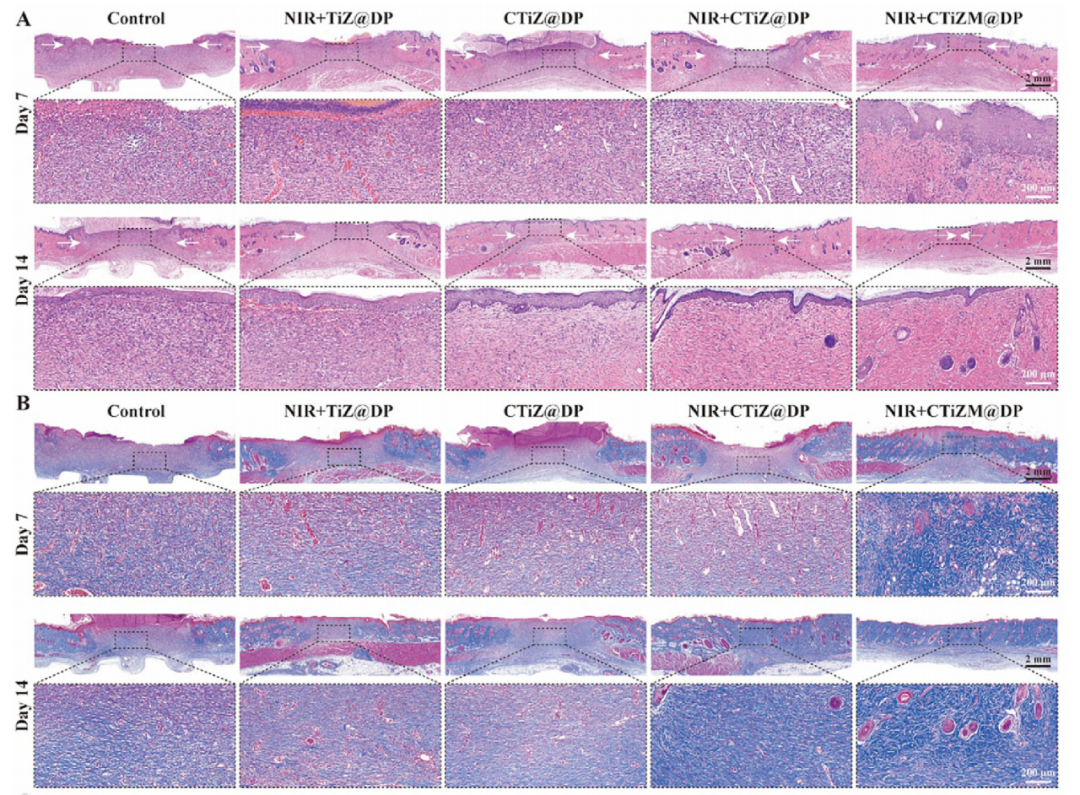
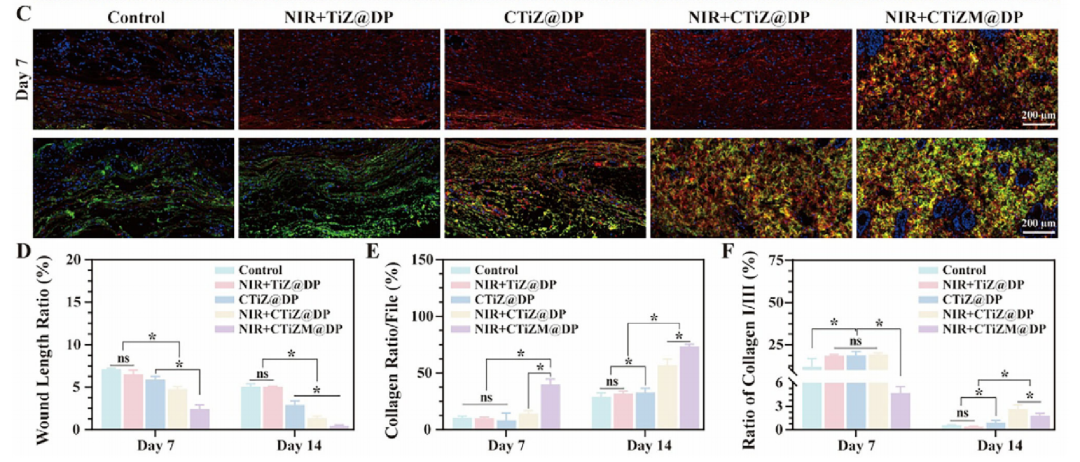
7
CTiZM@DP 光热水凝胶通过抑制 NF-κB 通路调控免疫微环境,促进创面愈合
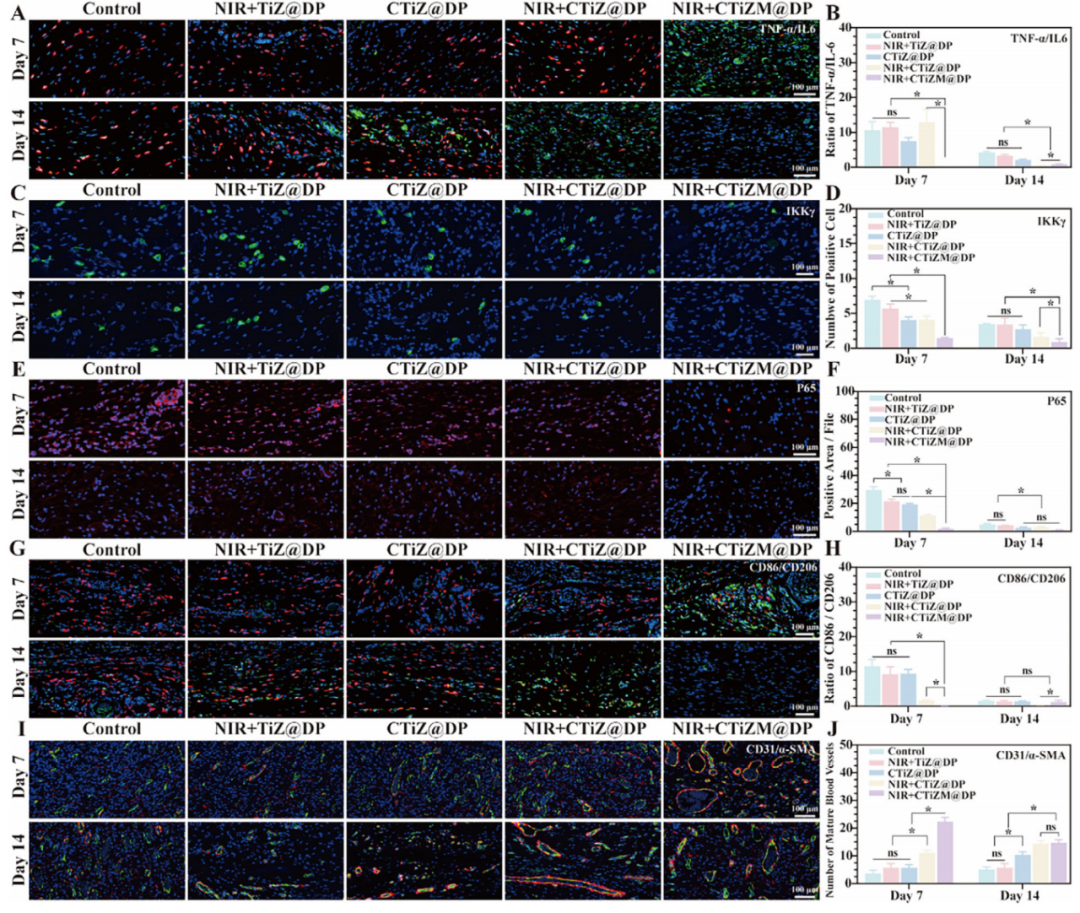
针对耐甲氧西林金黄色葡萄球菌(MRSA)感染糖尿病慢性创面的传统治疗存在靶向性差、易产生耐药性、难以兼顾抗菌与创面修复等局限,本研究设计构建了CTiZM@DP复合水凝胶治疗体系:以Ti₃C₂/ZnAl-LDH为原料制备空心TiZ纳米颗粒,经负载绿原酸、包裹凋亡中性粒细胞膜得到仿生NETs纳米颗粒CTiZM,再将其包封于温敏型DP水凝胶中,形成集温和光热效应、精准靶向、抗菌、免疫调节于一体的新型治疗平台。
该复合水凝胶在体内外实验中均展现出优异效能,可高效清除糖尿病创面的MRSA(包括巨噬细胞内的胞内菌),减轻感染引发的病理损伤与局部及全身炎症反应;同时能修复巨噬细胞免疫衰老、调控成纤维细胞表型,实现免疫微环境与再生微环境的双重重塑,最终显著加速糖尿病MRSA感染创面的愈合进程,且无明显全身毒性。
-
本研究提出的这一治疗策略,突破了传统抗生素的应用瓶颈,充分结合了纳米材料的特性与细胞仿生靶向设计的优势,为临床中耐药菌及敏感菌引发的糖尿病慢性感染创面治疗提供了全新的思路与可行的技术方案,具有重要的临床转化潜力。
END
往期推荐