【Cytiva】Xuri™ 生长因子
生长因子可以调节细胞许多方面的功能,包括增殖和分化。
在细胞治疗和研究应用中,生长因子广泛用于 T 淋巴细胞和其他原代细胞的扩增。Xuri™ IL-2、IL-15 和 IL-21 生长因子是根据USP <1043>“ 细胞、基因和组织工程产品的辅助材料 ” 的建议开发,并根据现行良好制造工艺 (cGMP) 指南进行生产。使用Xuri™ 生长因子,可以快速开发稳健且可重复的细胞治疗工艺。
快速工艺开发
每个批次的 Xuri™ 生长因子都包含明确的特定活性信息。基于活性信息,可实现培养基使用剂量的一致,将工艺过程的差异最小化。使用 Xuri™ 生长因子,您可以实现过程的标准化,实现可重复的细胞处理过程,无需对每个新批次的生长因子进行验证。
高质量
Xuri™ 生长因子的生产获得了 GMP 证书,并被发证机构定期认证。制造过程符合国际协调会议 (ICH) 相关指南。按照ISO13485 质量管理体系执行产品放行程序。根据 USP 指南对无菌性和内毒素水平进行检测。Xuri™ 生长因子旨在为体外应用提供高质量且安全的细胞产品。
符合 USP <1043> 标准
应对监管部门的监管要求时,合规全面的文件响应是关键。
为了帮助您评估和记录生产过程,每个 Xuri™ 生长因子都有一个全面的文档支持文件。这些支持文件遵循 USP <1043>“细胞、基因和组织工程产品辅助材料 1” 的指导方针。
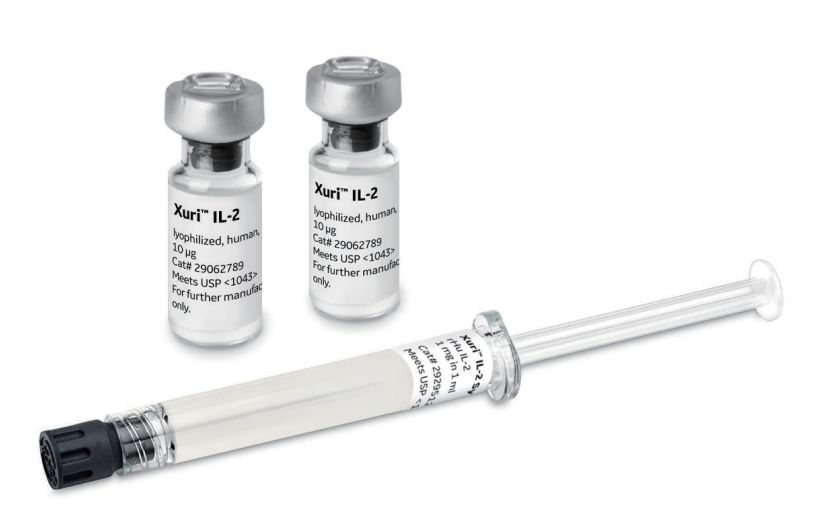
图 1. Xuri™ IL-2 可为 T 淋巴细胞提供可靠且高效的细胞扩增。两种形式可供选择:冻干粉剂 ( 左 ) 或溶液注射剂 ( 右 )。
Xuri™ IL-2
Xuri™ IL-2 ( 图 1) 是一种可靠的 T 淋巴细胞扩增试剂 ( 图 2 )。
产品可提供以下剂型:
• 瓶装冻干粉剂
• 注射器包装的稳定的溶液剂 ( 1 mg/mL )。注射剂包装有助于在不影响性能的前提下还能有效降低操作带来的污染风险Xuri™ IL-2 是经过充分验证的产品,与 Xuri™ 细胞扩增系统结合使用时性能良好。为了进一步加速您细胞扩增工艺的开发,我们可提供详细的 T 细胞扩增方案供您参考。该方案可在静态和灌流培养中提供可重复的细胞增殖效果 ( 图 2)。即使在培养 14 天后,大多数细胞仍处于分化的早期 / 中期 ( 基于 CD27和 CD28 表达模式 )( 图 3 ),没有明显细胞老化迹象。
*Xuri™ 生长因子产品符合 USP <1043>“ 细胞、基因和组织工程产品的辅助材料 ”,在适用于供应商的责任范围内。USP <1043> 的其他方面将由最终用户负责评估。Cytiva 无法在应用和治疗特定方面 ( 例如,在已完成治疗中使用、从已完成治疗中移除的评估,以及可能的生物相容性、细胞毒性或外来制剂测试 ) 满足 USP <1043> 的要求。
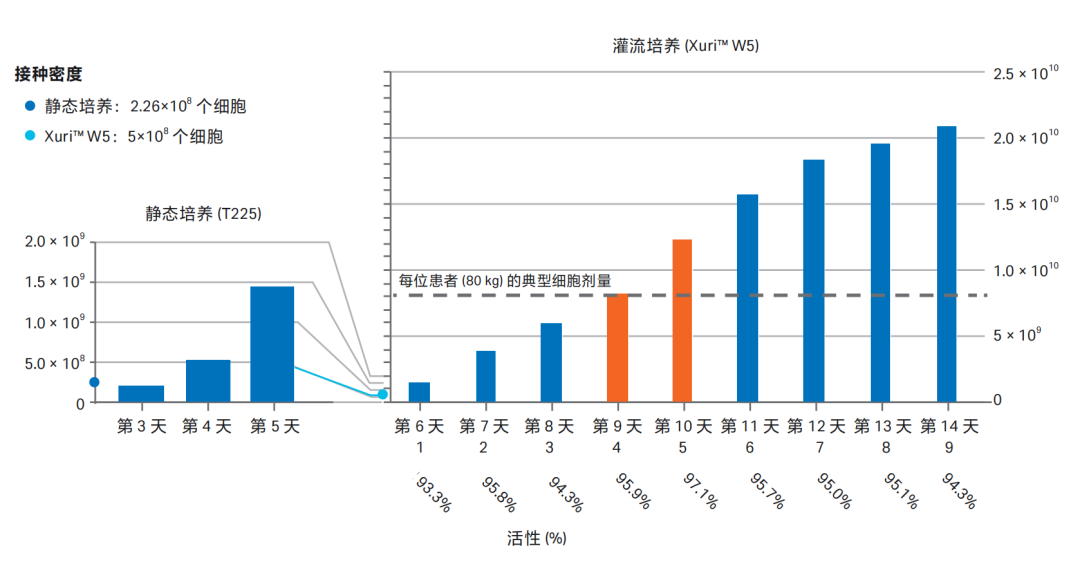
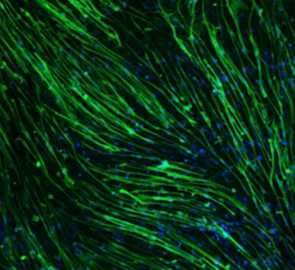
图 2. 从外周血中分离的 T 淋巴细胞最初在含有 5% 人血清和 200 IU/mL Xuri™ IL-2( 左图 ) 静态细胞培养瓶 ( T225 ) 中培养。通过抗体包被的磁珠激活细胞。从第三天开始计算细胞数,培养至细胞数量超过 2L Cellbag 一次性细胞培养袋接种所需的细胞数量 ( 5×108 )。然后将细胞转移到 Xuri™ 细胞扩增系统 W5 上,在灌流培养模式下再培养 9 天。培养基成分和 Xuri™ IL-2 浓度与静态培养相同 ( 见应用指南 28965052 )。每天进行细胞计数和活性分析。
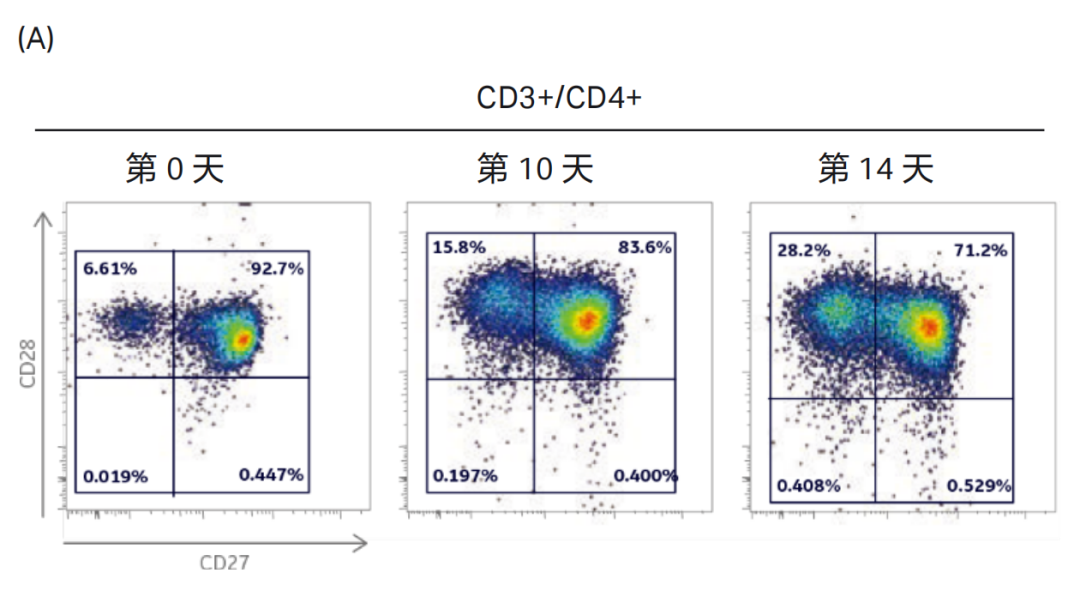
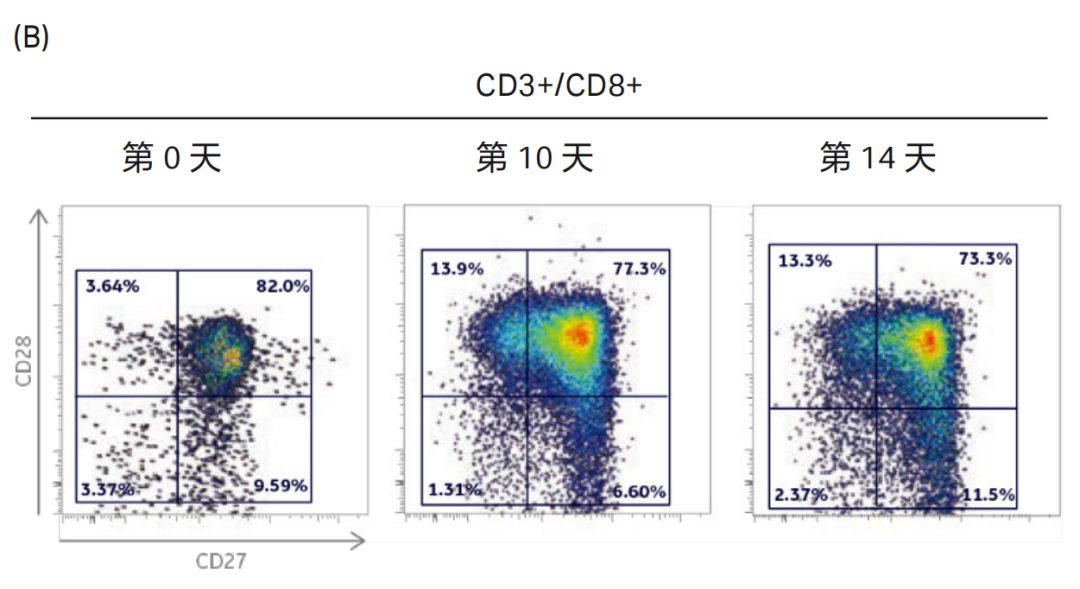
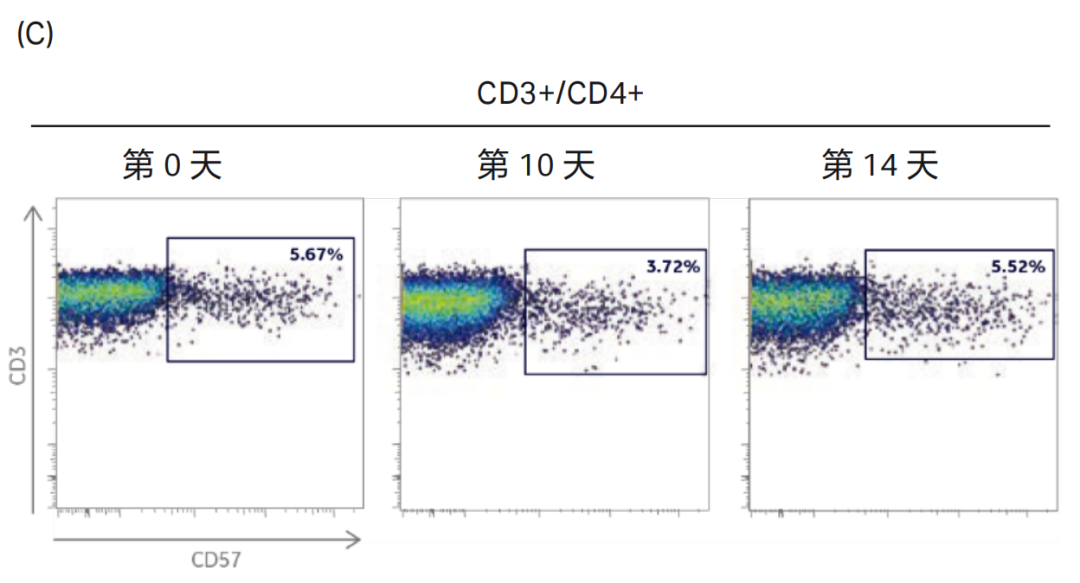
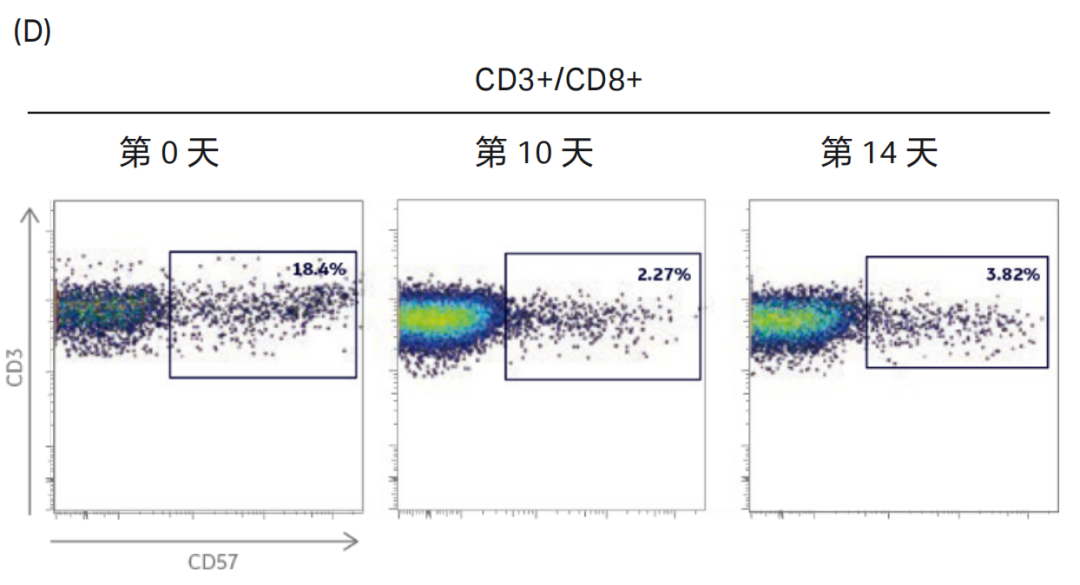
图 3. 在培养的第 0 天、第 10 天和第 14 天,对 Xuri™ W5 扩增系统中培养的 CD3+CD4+ 辅助性 T 细胞和 CD3+CD8+ 细胞毒性 T 细胞亚群的共刺激分子 CD28,CD27 及 CD57 的表达进行检测 ( 通过前向和侧向散射光对淋巴细胞进行圈门)。(A)CD3+CD4+ 辅助性 T 细胞中 CD28+ 和 CD27+ 细胞的比例;(B)CD3+CD8+ 细胞毒性 T 细胞中 CD28+ 和 CD27+ 细胞的比例;(C)CD3+CD4+ 辅助性 T 细胞中 CD57+ 细胞的比例;(D)CD3+CD8+ 细胞毒性 T 细胞中 CD57+细胞的比例;细胞表面分子 CD27 和 CD28 的表达能提示 T 细胞的分化状态。初始或早期分化的 T 细胞为 CD27+CD28+,效应 T 细胞为 CD27+CD28-或 CD27-CD28+,晚期效应或老化的 T 细胞为 CD27-CD28-。CD27 和 CD28 在培养 14 天后的 T 细胞上表达依然很高,提示细胞大部分都处于分化的早期 / 中期。CD57 是细胞老化的标记,流式结果显示三个时间点的 T 细胞上都没有明显的 CD57+ 细胞亚群。
Xuri™ IL-2 在培养基中的持久性
在整个培养过程中,生长因子的持续有效性是细胞扩增的关键要求。我们对两个不同温度下、两种不同浓度的 Xuri™ IL-2和竞品公司 IL-2 进行了连续 8 天的监测。酶联免疫吸附测定 (ELISA ) 数据显示,Xuri™ IL-2 在8天内一直维持稳定的浓度(图 4)。
注射器包装的 Xuri™ IL-2 的性能
我们对注射器包装的 Xuri™ IL-2 ( 三个批次)和冻干剂的 Xuri™IL-2 进行了性能对比。通过测量支持细胞生长的能力、细胞活性、表型 ( CD3 / CD4 / CD8 ) 和激活水平 ( CD25 ) 比较两者性能。
三批注射器包装的 Xuri™ IL-2 的细胞增殖 ( 图 5A) 和细胞活性( 图 5B) 的表现相近,且与冻干粉剂包装的功能一致。三个批次的注射器包装的 Xuri™ IL-2 在细胞表型和细胞活化状态的表现(图 5C) 与冻干粉剂包装的表现也相近。
在 Xuri™ 培养基中 Xuri™ IL-2 与竞品公司 IL-2 的稳定性和持续性比较。第 0 天调整浓度到统一剂量

图 4. 8 天内 IL-2 在 Xuri™ 扩增培养基 (EM) 中的稳定性变化情况。第 0天调整浓度到统一剂量。以 25 和 12.5 mg/mL 两种不同的浓度将符合GMP 要求的 Xuri™ IL-2 和 竞品公司 IL-2 加入含 5% 人 AB 血清的 Xuri™基础培养基中,置于 5% CO2 、37℃ 的湿化组织培养箱中。将含有 5%人 AB 血清 ( 含 Xuri™ IL-2 或 竞品公司 IL-2 ) 的 Xuri™ 基础培养基保存在 4℃环境下作为对照样本。。在第 0、1、2、3、5 和 8 天收集培养基,添加蛋白酶抑制剂,并将样本冷冻在 -80℃ 的冻存设备中,以备后续分析。采集所有时间点的样本后,对样本解冻,并使用 OptEIATM IL-2ELISA 试剂盒 (BD Biosciences) 确定 IL-2 的浓度。结果为平均值 ± 标准差,n=3。
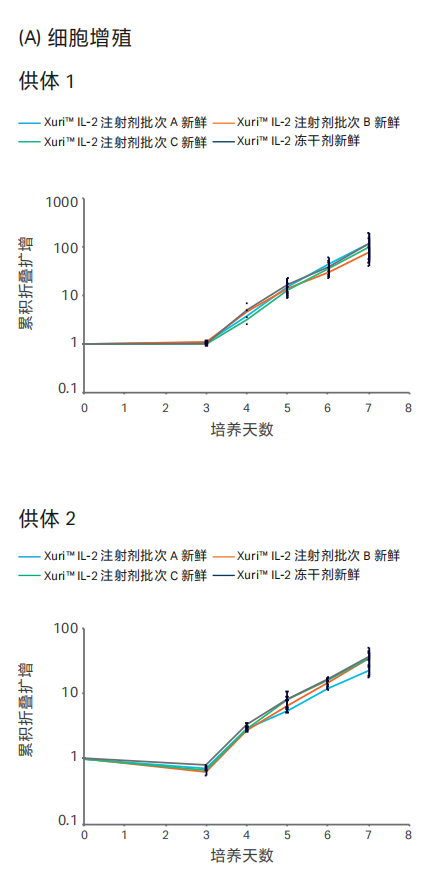
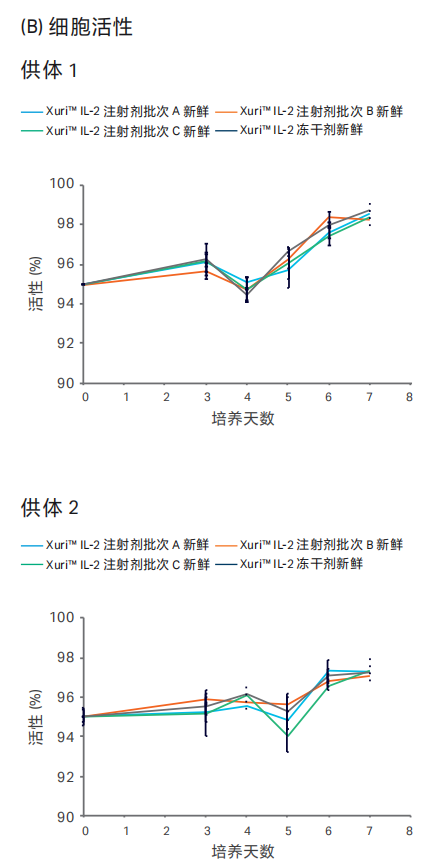
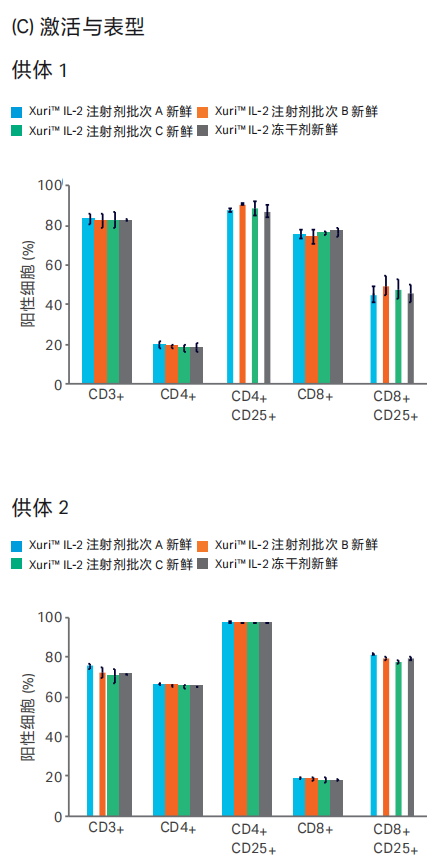
图 5. 三批注射器包装的 Xuri™ IL-2 ( 液体 ) 在 T 细胞扩增中的性能。冻干分剂包装的 Xuri™ IL-2 作为对照。(A) 细胞增殖 (B) 细胞活性 (C) 激活与表型。
人外周血单个核细胞 ( PBMC ) 从 2 个供体中获得。将 IL-2 ( 终浓度 350IU/ml) 添加到含 5% 灭活血清 (Gemini Bioproduct) 的 ImmunoCultTM XF T 细胞扩增培养基 (STEMCELL Technologies)。第 0 天,用 CD3/CD28/CD2 可溶性激活剂 ( STEMCELL Technologies ) 激活 T 淋巴细胞,并在温度为 37℃、CO2浓度为 5% 的 T-25 中培养 8 天。每天计数监测细胞扩增倍数及细胞活性。用染料标记抗体 (PerCP CyTM 5.5-CD3、V500-CD4、Alexa FluorTM 488-CD8和 PE-CD25) 对细胞染色,并使用 BD LSR FortessaTM 系统 ( 来自 Becton Dickinson 的抗体和流式细胞仪 ) 进行流式细胞分析。结果为平均值 ± 标准差,n=3。
Xuri™ IL-15
白细胞介素 15 (IL-15) 可调节人淋巴细胞的活化、增殖和分化。在培养过程中,用于 T 淋巴细胞和自然杀伤 (NK) 细胞的扩增。
Xuri™ IL-21
白细胞介素 21 (IL-21) 可调节人淋巴细胞的增殖和分化。在培养过程中,可用于诱导特定表型的 T 细胞亚群。
订购信息
产品 | 包装规格 | 代码编号 |
Xuri™ IL-2 注射剂,1 mg/mL(USP<1043> 仅供进一步生产使用 ) | 1 mg | 29295127 |
Xuri™ IL-2 ( USP<1043> 仅供进一步生产使用 ) | 10 μg | 29062789 |
Xuri™ IL-2 ( USP<1043> 仅供进一步生产使用 ) | 1 mg | 29062790 |
Xuri™ IL-15 ( USP<1043> 仅供进一步生产使用 ) | 40 μg | 29112116 |
Xuri™ IL-21 ( USP<1043> 仅供进一步生产使用 ) | 40 μg | 29112119 |
其他细胞品类
别划走,精彩继续

长按识别
添加一对一专属技术支持

扫码进群
咨询详细产品信息

点在看,传递你的品味